|
В предыдущих и в настоящей главе при рассмотрении
роли экспериментальных исследований для понимания процессов магматизма,
метаморфизма и, особенно, метасоматоза
подчеркивалась роль "растворов" или "флюидной
фазы" для ускорения всех реакций между минералами;
для транспорта вещества при процессах петро- и рудогенеза; как среды,
обеспечивающей вполне подвижное поведение ряда компонентов,
и во многих других случаях. Выше в данной главе показана неизбежность
их отделения от силикатных расплавов при кристаллизации. Присутствие флюидных
фаз в минералообразующих процессах фиксируется во включениях. На составе
пород и слагающих их минералов флюидная фаза отражается незначительно,
играя "роль певца за сценой". Содержание терминов "флюиды", "растворы"
и т.п. физико-химически очень неопределенное, хотя для геологов привычное
и интуитивно понятное. Как и всегда в таких случаях свободное применение
терминов может привести к путанице и, даже, к существенным ошибкам. Реально
речь обычно идет об обособленной в виде одной, двух, реже большего числа
фаз части общей системы, содержащей летучие и солевые соединения. Среди
них наибольшую роль в природных процессах играют H2O,
CO2 и хлориды K и Na,
в конкретных случаях существенное значение могут приобретать кислород,
фториды, фосфаты, бораты и др.
Система H2O - CO2 -
NaCl обычно рассматривается в качестве главной модельной
флюидной системы не только
потому, что содержит наиболее распространенные компоненты флюида, но и
как отражающая самые важные свойства подобного типа систем.
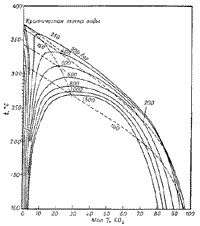 |
| Рис. 50. Изобарические кривые и критическая
кривая системы H2O - CO2. |
Однокомпонентные системы H2O
и CO2 ведут себя при высоких давлениях
и температурах принципиально сходно, хотя сами вещества сильно различаются:
вода - это полярный газ, углекислота - неполярный. При нормальных условиях
вода - жидкость, углекислота - газ. Оба вещества имеют на диаграмме Р
- Т (рис. 50) характерные критические
точки, выше которых наступает полная гомогенизация системы и вместо
пара или жидкости существует так называемый флюид, в котором отсутствует
ближний порядок в расположении молекул (как в газе), и в тоже время плотность
его высокая (как у жидкости). Кроме того, флюид практически несжимаем
(как жидкость). Флюид - это особое надкритическое
состояние вещества.
Для флюидных систем неприменимы традиционные закалочные методы. Состояние
систем, подобных рассмотренным, изучают методом PVT: заполняют автоклав
определенным количеством раствора, разогревают до необходимой температуры
и измеряют давление. Становится известным объем, занимаемый молем вещества
при данных РТ- параметрах. Точки перегибов зависимостей V от Р и Т отвечают
фазовому переходу пар-жидкость.
Во многих более сложных (с двумя компонентами
и более) системах имеются области, в которых флюид сосуществует с более
плотной жидкой фазой. В системе H2O-CO2
(рис. 50) при давлении 1 кбар
и невысоких температурах (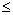 400оС)
существует область несмесимости, которая
с повышением температуры замыкается. С повышением давления до 2,5 кбар
этот купол расслоения смещается в область более низких температур - то
есть с увеличением давления система становится более идеальной. При давлениях
> 3 кбар экспериментальные данные для этой
системы противоречивы. 400оС)
существует область несмесимости, которая
с повышением температуры замыкается. С повышением давления до 2,5 кбар
этот купол расслоения смещается в область более низких температур - то
есть с увеличением давления система становится более идеальной. При давлениях
> 3 кбар экспериментальные данные для этой
системы противоречивы.
 |
|
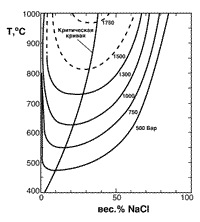
Рис. 51. Изобарическая (Т-Х) проекция сосуществующих
фаз в системе H2O - NaCl, установленая при изучении
синтетических флюидных включений (по данным Р.Боднара, С.Бернема,
С.Стернера)
|
Фазовые отношения в системе H2O
- NaCl показаны на рис.
51. В ней при давлении 1 кбар также имеется
двухфазовая (пар + жидкость) область. В отличие от системы с СО2,
она замыкается в сторону низких температур, давая критическую точку около
600оС. С повышением давления область пар + жидкость смещается
в область высоких температур и при Р=3 кбар отсутствует при температурах,
меньших 1000оС. Таким образом, с повышением температуры (при
Р 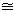 0.1 - 2 кбар)
неидеальность системы увеличивается , в то время как с повышением давления
смесь вода - соль становится более идеальной (сужается и исчезает поле
пар + жидкость). 0.1 - 2 кбар)
неидеальность системы увеличивается , в то время как с повышением давления
смесь вода - соль становится более идеальной (сужается и исчезает поле
пар + жидкость).
Исследования расслоения в системе Н2О
- NaCl, показали, что при параметрах гетерогенного состояния
системы осуществляется реакция высокотемпературного гидролиза:
NaCl + H2O = NaOH + HСl. Система,
таким образом, оказалась не двухкомпонентной. Кислота обогащает "паровую"
фазу, а щелочи концентрируются в жидкой (высокосолевой) фазе гетерогенной
флюидной системы.
В системе H2O - CO2
- NaCl (рис. 52)
с повышением давления поле существования гомогенного
флюида расширяется, повышение температуры оказывает противоположное
влияние. Экспериментальные данные при
высоких давлениях (Р  6 кбар)
пока отсутствуют. 6 кбар)
пока отсутствуют.
Методически явления несмесимости изучают
путем пробоотбора: из вертикально расположенного автоклава отбирают пробы
раствора из верхней и нижней части, анализ этих проб позволяет судить
о фазовом состоянии гидротермального раствора и
о составах сосуществующих фаз. Сходным образом синтез флюидных включений
в кристаллах кварца на разной высоте автоклава позволяет использовать
их как своеобразные пробоотборники. Кроме того, если при синтезе захватываются
комбинированные (расслоенные) включения, в последних
как в прозрачных автоклавах можно непосредственно наблюдать фазовые переходы
в водно-солевой системе при их нагревании (или охлаждении). Используется
также метод изучения катионообменных реакций в системе минерал (твердый
раствор) - флюид типа: 2NaAlSi3O8
+ [BaCl2]fl 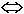 BaAl2Si2O8
+ 4SiO2 + 2[NaCl]fl(. Отстраиваются
изотермы составов сосуществующих фаз (минерала и флюида) - рис.
53. Изменения фазового состояния флюида отражаются
на изотерме в виде особых точек - переломов, изменений наклона и т.п. BaAl2Si2O8
+ 4SiO2 + 2[NaCl]fl(. Отстраиваются
изотермы составов сосуществующих фаз (минерала и флюида) - рис.
53. Изменения фазового состояния флюида отражаются
на изотерме в виде особых точек - переломов, изменений наклона и т.п.
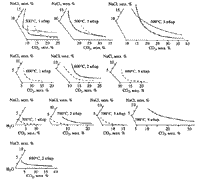 |
| Рис. 52. Положение области несмесимости
в системе Н2О - СО2 - NaCl при 500 -
7000 С и Р=1-5 кбар по данным изучения разными авторами
синтетических флюидных включений. |
Высокоплотным водносолевым фазам
с тем или иным содержанием алюмосиликатной составляющей в геологической
литературе давно придавалось большое значение в концентрации и переносе
рудного вещества, при образовании пегматитов, рудных и нерудных жил
и некоторых других образований.
Им давались названия "расплавы-растворы", "расплавы-рассолы",
"рудные магмы", "гидротермальная рапа",
"тяжелые флюиды", "флюидные расплавы". Экспериментально
они впервые были получены Ф.Смитом в 40-е годы при моделировании образования
пегматитов, затем обнаружены при выращивании кристаллов кварца в гидротермальных
условиях под названием "тяжелая фаза" (в отличие от легкого флюида накапливающаяся
в нижней части автоклава).
Как уже указывалось в главе V-1, концепция концентрирования рудного
вещества водными флюидами (гидротермальная теория) столкнулась с трудностями,
связанными с тем, что экспериментально определенные значения растворимости
практически всех рудных и породообразующих компонентов в них оказались
чрезвычайно низкими. Делались расчеты, показывающие, что для отложения
вещества одной рудной жилы через трещину необходимо пропустить количество
водного флюида, равное объему Средиземного моря (или годичному стоку Волги).
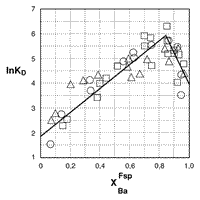 |
| Рис. 53. Зависимость величины логарифма
коэффициента распределения бария (InK) (усредненные значения ) от
состава плагиоклаза в равновесии с водно-солевым флюидом при 600 и
8000С. |
Необходимо оговориться, что данные низкой
растворимости большинства породообразующих и рудных компонентов во флюидах
относится к условиям земной коры (давлений до 10
килобар). Как уже обсуждалось выше, для мантийных условий
перенос вещества водными растворами может быть весьма эффективным, а для
глубин более 100 км по-видимому отсутствует различие между флюидами и
расплавами. Относительно окисленная природа мантии, основанная на термодинамическом
анализе равновесий минералльных парагенезисов включений в базальтах, предположительно
захваченных в мантии, показывает что значения летучести кислорода при
их формировании соответствуют условиям стабильности H2O
+ CO2, H2O + карбонаты.
Расчеты подтверждаются обычным присутствием плотной углекислоты во флюидных
включениях вероятных пород верхней мантии, карбонатов и воды - в микровлючениях
в природных алмазах.
Образование фаз флюидных
расплавов может быть весьма эффективным механизом дифференциации
вещества во всех эндогенных процессах, т.к. сепарация
жидких фаз осуществляется легче, чем, например, твердых фаз при фракционной
кристаллизации. Способы их генерации могут быть разнообразны. Возможна
гетерогенизация первично однородного флюида в силу изменившихся внешних
условий, например, кипение при декомпрессии, вызванной трещинообразованием.
Другим способом может быть высаливание - гетерогенизация вследствие добавления
к гомогенной смеси H2O, CO2
и NaCl малорастворимого компонента (CO2
или NaCl). В главе II-1
уже рассмотрен механизм, связанный с кристаллизацией, накоплением солевых
компонентов в остаточном расплаве и с их ограниченной растворимостью.
Кратко рассмотренные особенности "флюидных", т.е. состоящих
из летучих и солевых компонентов систем намечают только самые общие особенности
их физико-химии. Водносолевые системы изучены пока явно недостаточно.
С другими солями фазовые отношения принципиально похожи, но параметры
температуры и давления могут существенно отличаться. Серьезным недостатком
подобного рассмотрения является искусственное расчленение системы и выделение
из нее "флюидной части". В состав фаз последней могут в существенных количествах
входить компоненты другой - "силикатной" части. Примером может служить
фторсодержащая система, солевая фаза которой сложена алюмофторидами. Имеются
данные о вхождении в эти фазы и других породообразующих компонентов, в
том числе и кремния, особенно при высоких давлениях.
Процессы эндогенного минералообразования с участием флюидных
фаз (метасоматоз, метаморфизм,
рудообразование) и сопровождающее их перемещение
химических компонентов происходят в природе в специфических условиях тонкопористых
сред.
Экспериментально показано, что активности
Н2О и СО2
в поровом флюиде (размер пор 10-1-10-3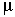 m) и в свободном объеме отличаются в 1,5-4 раза в зависимости
от Т, Р и диаметра пор. В первом приближении коэффициенты активности в
порах
m) и в свободном объеме отличаются в 1,5-4 раза в зависимости
от Т, Р и диаметра пор. В первом приближении коэффициенты активности в
порах 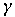 СО2пор>
1> СО2пор>
1> 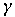 Н2Опор,
и, следовательно, мольные доли СО2
и Н2О в поровом растворе
будут соответственно ниже и выше,чем определенная из минеральных равновесий.
"Сухие" метаморфизм и выплавление магм могут быть связаны с флюидами,
не столь уж бедными водой, но с низкой ее активностью.
Н2Опор,
и, следовательно, мольные доли СО2
и Н2О в поровом растворе
будут соответственно ниже и выше,чем определенная из минеральных равновесий.
"Сухие" метаморфизм и выплавление магм могут быть связаны с флюидами,
не столь уж бедными водой, но с низкой ее активностью.
В тонкопористой среде коэффициенты
диффузии хлоридов K, Na, Ca, Mg, Fe, Al в 0,5-5,5
раз (в зависимости от Т, концентрации раствора, размера пор) меньше, чем
в свободном объеме водного раствора, хотя порядок величин в обоих случаях
10-5 см2/с. Они слабо
зависят от давления и отчетливо (в пределах 0.5-1 порядка) - от диффундирующего
иона, возрастая в последовательности: Al, Si, Ca, Mg, Fe, Na,
K. Для сравнения: коэффициенты диффузии в кристаллических решетках
алюмосиликатов при 100-800оС имеют порядок 10-20-10-10
см2/с; в водно-альбитовом расплаве
при 1000оС для SiO2, Al2O3,
P2O5 близки к 10-11,
для СаО, MgO, FeO лежат между 10-8 и 10-9,
а для Na2O, K2O, H2O, HF
- около 10-7, коэффициент диффузии
СО2 в воздухе 0,16 см2/с.
 |
| Рис. 54. Схематическая диаграмма,иллюстрирующая
фильтрацию электролитов через тонкопористые фильтры. |
Другой очевидный механизм гидротермального транспорта
в земной коре - это фильтрация. При просачивании
растворов через тонкопористые имеет место фильтрационный эффект.
Эксперименты показали, что при инфильтрации растворов происходит закономерное
изменение концентраций растворенных веществ. Оно слишком велико, чтобы
быть результатом сорбции и должно зависеть от динамических факторов. Фильтрационный
эффект заключается в различной скорости инфильтрации катионов и анионов,
которая сопряжена с изменением концентрации Н+
и (ОН)-, что вызывает кислотно-основную
дифференциацию растворов. Если поверхность минералов в породах заряжена
отрицательно (как это имеет место у большинства из них), то инфильтрация
кислотных компонентов происходит быстрее с накоплением их в голове потока.
Градиенты давления способствуют более быстрой инфильтрации ионов с положительным
парциальным молярным объемом, что характерно для анионов многих кислот.
Наоборот, ионы с положительным зарядом и отрицательным парциальным мольным
объемом (Ca+2, Mg+2, Zn+2,
Pb+2, Cu+2, Fe+2, Fe+3┘)
замедляются в потоке и их концентрации возрастают в его тыловых частях
(рис.
54). Фильтрационный эффект имеет преимущественно
электрокинетическую природу, усложненную бародиффузией,
хемодиффузией, а также особыми условиями вязкого
течения через тонкопористую среду. Другую сторону того же явления описывает
"мембранный" эффект: задержка в фильтрации
компонентов и возрастание концентрации на границе с труднопроницаемым
слоем, геологическим следствием которого является отложение руд перед
экранами.
Закон Дарси линейно связывает
фильтрационный поток с константой проницаемости и градиентом давления.
Проницаемость измеряют в единицах дарси (для низкопроницаемых горных пород
обычно в миллидарси). 1Д соответствует потоку жидкости 1 см3/с
через 1 см2 сечения при градиенте давления 1
атм/см и вязкости жидкости 1 сПз. Уровень проницаемости 10-3
мД - минимальный, при котором становится возможной циркуляция растворов
с преобладанием инфильтрационного переноса над диффузионным. У большинства
пород в образцах, лишенных микротрещин, проницаемость измеряется в 10-4-10-6
мД. Они представляют трудно преодолимые преграды для движения гидротермальных
флюидов.
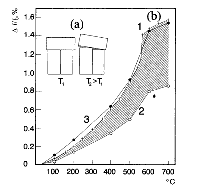 |
| Рис. 55. Тепловое разуплотнение горных
пород. |
Существование в природе мощных потоков флюидов
сквозь толщи горных пород объясняется тепловым разуплотнением
горных пород. Разуплотнение происходит при нагревании столь же непременно,
как и тепловое расширение. Экспериментально оно получено при температурах
от 20 до 700оС при атмосферном давлении, в автоклавах под давлением
H2O, CO2, Ar (pfl=psol=1.0
kbar) и при превышении давления на твердый каркас над флюидным. Интенсивность
эффекта возрастает с температурой и увеличивается от ультраосновных пород
к кислым. Реальное тепловое расширение почти в 2 раза выше, чем расширение
слагающих породы минералов (рис. 55).
Сущность эффекта теплового разуплотнения - образование дополнительного
порового пространства в результате раскрытия трещин по границам зерен.
Оно наиболее сильно проявлено у пород, в состав которых входит кварц (благодаря
различию коэффициентов расширения у разных минералов), и у мраморов (из-за
анизотропии свойств карбонатов). У пород, сложенных
одним изотропным минералом (гранатовые скарны, магнетитовые
руды) разуплотнение отсутствует. После остывания сохраняется остаточное
расширение. В присутствии воды степень разуплотнения возрастает благодаря
адсорбционному понижению прочности межзерновых контактов
в воде, являющейся поверхностно-активной средой. С разуплотнением уменьшается
объемный вес, прочность, скорости прохождения упругих
волн, увеличивается пористость, фактор электропроводности
и проницаемости (рис. 56). Температура
увеличивает проницаемость на 2-2,5 порядка от 200
до 600оС, давление - уменьшает на 2 порядка от 50 до 800 бар.
Проницаемость пород обусловлена в основном межзерновой пористостью, образующей
связанную сеть транспортных каналов.
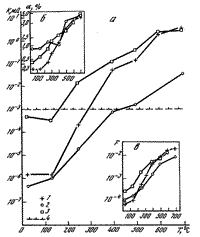 |
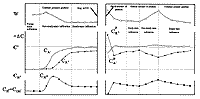
| Рис. 56. Изменение транспортных характеристик
горных пород после нагрева в гидротермальных условиях |
Элементарной ячейкой является капиллярный канал
непостоянных сечения, длины и формы: от тонкой щели до круглой трубы.
С повышением температуры в гранитах снижается доля узких (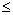 0,1 мкм) микротрещин, преобладающих в исходной породе, и постепенно возрастает
- более широких (0,1-10 мкм). Средняя длина возрастает при нагреве до
700оС от 0,1-20 мкм до 10-180 мкм. После нагрева в воде ширина
микротрещин больше при одинаковой линейной плотности. В гидротермальных
условиях появляются приконтактовые зоны узких (0,2-10 мкм) кайм тонко
диспергированного материала, отсутствующих при другом нагреве.
0,1 мкм) микротрещин, преобладающих в исходной породе, и постепенно возрастает
- более широких (0,1-10 мкм). Средняя длина возрастает при нагреве до
700оС от 0,1-20 мкм до 10-180 мкм. После нагрева в воде ширина
микротрещин больше при одинаковой линейной плотности. В гидротермальных
условиях появляются приконтактовые зоны узких (0,2-10 мкм) кайм тонко
диспергированного материала, отсутствующих при другом нагреве.
Расчеты, подобные приведенным выше, проводятся
при допущении идеальности газовых смесей. Они могут быть в дальнейшем
скорректированы. Появились экспериментальные данные об отклонениях смесей
от идеальных, в том числе и рассмотренных смесей H2O
c CO2, CH4, H2, O2.
Оказалось, что величина избыточного объема смешения (разница между реальным
и аддитивным объемами смеси - см. главу V-3)
в зависимости от давления характеризуется максимумом. Объемные свойства
бинарной газовой смеси определяются компонентом с более высокой критической
температурой, что связывают с процессами молекулярной
кластеризации вблизи критических параметров.
Дополнительная литература.
Маракушев А.А. Происхождение и эволюция Земли и других
планет Солнечной системы. Изд. "Наука", М, 1992, 206 с.
Лебедев Е.Б., Хитаров Н.И. Физические свойства магматических
расплавов. Изд. "Наука", М, 1979, 200 с.
Персиков Э.С. Вязкость магматических расплавов. Изд.
"Наука", М, 1984, 160 с.
Fluids in the crust. Chapman & Hall, London, 1995,
323 pp.
|

