Метод количественной оценки состава и
концентрации исходного раствора рассмотрен нами
[Иванов и др., 1979; Иванов, Борисов, 1980]
на примере моделирования метасоматический
зональности в простейших колонках кислотного
выщелачивания пород. В основу моделирования
положены принципы, выдвинутые Д.С.Коржинским [1969]: 1) принцип локального
равновесия между породой и поровым раствором;
2) принцип дифференциальной
подвижности компонентов при метасоматизме; 3) принцип кислотно-основного
взаимодействия между воздействующим раствором и
породой.
Согласно теории метасоматической зональности
Д.С.Коржинского, при инфильтрационном
метасоматизме в стационарных условиях про
исходит постепенное разрастание зон в колонке
без качественного изменения минерального
состава и объема породы; зоны разделены между
собою резкими фронтами замещения и
характеризуются последовательным уменьшением
числа сосуществующих в них минералов вплоть до
перехода к мономинеральной тыловой зоне.
Строение колонки не зависит от кинетики
протекающих в ней реакций, а определяется
локальными равновесиями на фронтах растворения и замещения
минералов, т.е. на границах между соседствующими
зонами.
Сущность метода
расчета локальных равновесий на этих фронтах
заключается в следующем. За основу берется
детально изученная природная метасоматическая
колонка с фиксированными минеральными
ассоциациями в зонах и известным рядом
дифференциальной подвижности компонентов в
ней. Каждая из зон в этой колонке рассматривается
как открытая система с вполне подвижными
компонентами, для которой однозначно
устанавливается набор независимых параметров
(факторов равновесия), исходя из того, что все эти
зоны однозначно связаны в колонке между собою
режимом дифференциальной подвижности
компонентов. При последовательном сопоставлении
фазовых составов соседствующих открытых систем
с вполне подвижными компонентами и
контролирующих их факторов равновесия легко
выводятся граничные реакции на фронтах
замещения между зонами в колонке [Иванов,
Борисов, 1980]. Далее равновесия этих реакций
рассчитываются термодинамически и изучаются
экспериментально, что позволяет реставрировать
состав исходного раствора и его изменение вдоль
колонки от зоны к зоне, с каждой из которых он
находится в локальном равновесии.
Рассмотрим простейшую одноактную
метасоматическую колонку формации
кварц-серицитовых метасоматитов, связанную с
изменением гранитов, в которой на фронтах
замещения (на границах между зонами) происходит
инконгруэнтное растворение минералов
алюмосиликатного состава:
Кв  |
Кв+Сер  |
Кв+Сер+Кпш  |
Кв+Сер+Кпш+Аб  |
Кв+Сер+Кпш+Аб+Хл |
| (5) |
(4) |
(3) |
(2) |
(1)- номера зон. |
По сравнению с природными колонками
здесь отсутствуют зоны с рудным минералом (пирит,
гематит, магнетит) и с кальцитом, и зональность не
доводится до исходного гранита.
Для стационарных условий (постоянные
значения Т, Р, состава и скорости просачивания
раствора) между зонами в колонке устанавливаются
следующие граничные реакции, выведенные на
основе анализа парагенезисов минералов:
1-2:Хл+Кпш+10Н+ = 3Кв+Сер+nMg2++(5
- n)Fe2++8H2O;
2-3:Аб+0.5Кпш+H+ = 3Кв+0.5Сер+Na+;
3-4:1.5Кпш+H+ = 3Кв+0.5Сер+K+;
4-5:Сер+10H+ = 3Кв+3Al3++K++6H2O.
В этих реакциях
нет никаких указаний на то, какова должна быть
солевая нагрузка раствора, которая
устанавливает ряд дифференциальной подвижности.
Это может быть галоидный, карбонатный,
сульфидный, сульфатный и другой раствор или
раствор более сложного смешанного состава. В
этом и есть сущность конвергенции метасоматизма,
когда одна и та же метасоматическая колонка
может быть получена под действием разных
исходных солевых растворов, содержащих необходимый набор
металлов (катионов).
Расчеты
равновесного состава раствора были проведены
при 300oС и 0.1-1 кбар для четырех зон, начиная
с тыловой, представленной чистым кварцем, и в
нескольких случаях для пяти зон. В качестве
твердых фаз в систему были введены все минералы,
которые могут образоваться при заданном валовом
составе системы. В расчетах участвовали
следующие частицы: Н+, ОН-, К+, КСl0, КНСО30, КСО3-, Na+, NaCl0,
NaHCO30, МgСО30,
HCl0, Cl-, СО32-, НСО3-, Н2СО30,
Al3+, Al(OH)2+, Al(OH)2+, Al(OH)30,
AlCl2+, H3SiO4-, H4SiO40.
В основу моделирования положена схема
последовательного насыщения исходного раствора
компонентами минеральных ассоциаций в зонах
заданной колонки, с учетом баланса вещества, при
прохождении этого раствора сквозь колонку.
Выделим в каждой зоне колонки участок массой в 1
кг. Примем нормативный минеральный состав в
зонах эталонной колонки кварц-серицитовых
метасоматитов, как представлено в таблице
2.1.
Далее полагаем,
что выделенные участки отдельных зон могут
взаимодействовать с 1 кг воды и солями,
растворенными в ней (кинетические аспекты
реакций не рассматриваются). Теперь
последовательно будем проводить испытуемый
раствор через колонку. Покажем это на конкретном
примере. Например, исходным раствором является
чистая вода. На первом этапе проводим расчет
взаимодействия 1 кг Н2О с 1 кг кварца из тыловой зоны. Равновесный с
кварцевой зоной раствор полностью перемещаем
(т.е. воду с некоторым количеством кремнекислоты)
в Кв+Сер зону, где также достигается равновесие.
Затем равновесный с Кв+Сер зоной раствор
поступает в зону Кв+Сер+Кпш. Так, последовательно
перемещая раствор из зоны в зону, можно
проследить изменения на границах зон (скачки)
состава равновесного раствора. Следует отметить,
что в данном исследовании впервые был применен
при расчетах метод ступенчатых проточных
реакторов [Иванов, Борисов, 1980],
который позже был значительно развит и
использован в многоволновом варианте при
анализе сложных гидротермальных систем [Гричук, Борисов, 1983; Гричук и др., 1985;
Барсуков, Борисов, 1987- 1992].
Проведя подобные реакционные
взаимодействия с растворами, содержащими
различные компоненты в нескольких
концентрациях, мы можем определить граничные
варианты растворов, при которых тип зональности
не меняется, а также проверить выделенные выше на
основе анализа парагенезисов граничные реакции
на фронтах между зонами, поскольку нам известны
начальные (заданные) и конечные (полученные из
расчета) количества этих минералов. Таким
образом мы можем оценить пределы составов
исходных растворов, которые привели к
зональности данного типа.
Были изучены
следующие исходные растворы: H2O;
H2O+НСl; H2O+КСl; H2O+КСl+NаСl;
H2O+КНСО3 . Для каждого из них были
получены на ЭВМ локальные равновесия как это
излагалось выше, с выдачей необходимых данных,
включающих баланс вещества в системе; состав и
концентрацию раствора, равновесного с
минералами зон; рН и ионную силу раствора.
Результаты моделирования зональности по твердым
фазам представлены в таблице 2.2.
При воздействии
чистой воды и раствора H2O+HCl в зоне Кв+Сер проходит реакция Сер Кл, т.е. образуется колонка
типичных аргиллизитов (и вторичных кварцитов).
Между кварцевой и кварц-серицитовой зонами
появляется кварц-каолинитовая зона. Кл, т.е. образуется колонка
типичных аргиллизитов (и вторичных кварцитов).
Между кварцевой и кварц-серицитовой зонами
появляется кварц-каолинитовая зона.
При воздействии
галоидного раствора H2O+KCl с концентрациями от n.10-6 до n.10-1 m можно выделить три типа
локальных равновесий. При mKCl = n.10-6- n.10-2 полностью воспроизводится
эталонная колонка. Но при mKCl > n.10-3в зоне
Кв+Сер+Кпш+Аб происходит растворение альбита по
реакции Аб Кпш, т.е.
идет вынос альбита из колонки и замещение его
калиевым полевым шпатом. Увеличение
концентрации КCl до 5.10-1 m приводит к замещению зоны Кв+Сер. Вместо
нее становится стабильной зона Кв+Кпш, что
отвечает природным гумбеитам. Кпш, т.е.
идет вынос альбита из колонки и замещение его
калиевым полевым шпатом. Увеличение
концентрации КCl до 5.10-1 m приводит к замещению зоны Кв+Сер. Вместо
нее становится стабильной зона Кв+Кпш, что
отвечает природным гумбеитам.
Поэтому оптимальным для эталонной колонки
является исходный раствор, имеющий концентрацию
mKCl = n.10-6-
n.10-3 m.
Введение NaCl в
исходный раствор, содержащий КCl (mKCl + mNaCl = 0.1
m), также приводит к нарушению эталонной колонки.
Как видно из таблицы 2.2,
преобладание калия над натрием приводит к
гумбеитовой зональности, преобладание натрия
над калием - к кварцевым альбититам.
Для оценки роли
карбонатного раствора были просчитаны три
состава раствора H2O+КНСО3при PCO2 = 1 атм. Эталонная колонка
остается стабильной при воздействии раствора с mKHCO3 = 10-3. При mKHCO3 = 10-5 в зоне Кв+Сер появляется
каолинит, а при mKHCO3 > 10-3 в этой же зоне образуется
калиевый полевой шпат. Поскольку два последних
варианта сразу же отходят от эталонной колонки,
то расчет реакций в них с последующими зонами не
представляет интереса.
Таким образом, из
всех испытанных исходных растворов только два
раствора, H2O+КCl и H2O+КНСО3 позволяют полностью моделировать колонку
кварц-серицитовых метасоматитов, причем, в
довольно узких интервалах концентраций.
Поскольку с галоидным раствором были проведены
более полные исследования, остановимся на
характеристике этого раствора, находящегося в
локальном равновесии с минеральными
ассоциациями в зонах эталонной колонки.
В таблице
2.3 показано изменение состава исходного
раствора H2O+КCl с mKCl = 10-5при его последовательном
перемещении через зоны этой колонки в условиях,
когда скорость стационарного потока
инфильтрации превышает скорость диффузии
компонентов в поровом растворе. Приведены
валовые концентрации элементов в этом растворе
по мере его насыщения по отношению к минералам
каждой из зон, pH и баланс вещества между твердыми
фазами и раствором. В более наглядном виде данные
таблицы 2.3 представлены на рисунке 2.1.
 |
| Рис. 2.1. Валовые концентрации элементов и рН
раствора, равновесного с минеральными
ассоциациями в зонах колонки кварц-серицитовых
метасоматитов |
Из таблицы 2.3 и
рисунка 2.1 видно, что реализуется ступенчатое
насыщение раствора Al и K на границах зон 5-4 и 4-3
за счет инконгруэнтного растворения
соответственно серицита и калиевого полевого
шпата; натрием - на границе зон 3-2 за счет
инконгруэнтного растворения альбита и магнием -
на границе зон 2-1 за счет инконгруэнтного
растворения хлорита, что полностью подтверждает
дифференциальный ряд подвижности компонентов в
колонке кварц-серицитовых метасоматитов, но уже
на количественной основе. Концентрация кремния в
растворе во всех зонах остается практически
постоянной, так как она фиксируется буферной
твердой фазой - кварцем, который присутствует во
всех зонах (избыточный минерал). Щелочность
раствора (pH) возрастает в направлении от тыловой
зоны к головной. Проявляется кислотно-основное
(щелочное) взаимодействие - раствор в зонах
становится ступенчато более щелочным по
сравнению с исходным, а порода в зонах - более
кислой (кремнекислотной) по сравнению с гранитом.
Концентрация Si в растворе является максимальной
и весьма незначительно возрастает при повышении
рН раствора (возрастает растворимость кварца).
Концентрация Al ниже концентрации Si на 3-4 порядка
и понижается с повышением рН раствора. Причем в зонах с двумя (и
более) твердыми фазами, содержащими алюминий,
концентрация последнего в растворе оказывается
фиксированной (3.077.10-6 моль/1000 г H2O).
В зонах с двумя (и более) калий-содержащими фазами
равновесный раствор сохраняет фиксированное
отношение 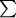 К/ К/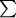 Н, что объясняется буферным
действием моновариантной ассоциации минералов
Кв+Сер+Кпш. Концентрации Na и Mg в растворе
стабилизируются буферным действием альбита и
хлорита соответственно. Следует подчеркнуть, что
равновесная концентрация Na в головных зонах на
порядок выше, чем концентрация калия, хотя натрий
не вводился в исходный раствор. Хлор является
"проходящим" компонентом, и его
концентрация в растворе не изменяется. Потеря в
весе минералов включает их инконгруэнтную
растворимость и образование других стабильных минералов в
соответствии с уравнениями граничных реакций
между зонами. Н, что объясняется буферным
действием моновариантной ассоциации минералов
Кв+Сер+Кпш. Концентрации Na и Mg в растворе
стабилизируются буферным действием альбита и
хлорита соответственно. Следует подчеркнуть, что
равновесная концентрация Na в головных зонах на
порядок выше, чем концентрация калия, хотя натрий
не вводился в исходный раствор. Хлор является
"проходящим" компонентом, и его
концентрация в растворе не изменяется. Потеря в
весе минералов включает их инконгруэнтную
растворимость и образование других стабильных минералов в
соответствии с уравнениями граничных реакций
между зонами.
Рассмотренные варианты, естественно,
не охватывают всего многообразия возможных
исходных растворов, моделирующих рассмотренную
эталонную зональность.
|

