Развитие точного естествознания, к которому стремится физическая геохимия, неразрывно связано со все более широким и разнообразным применением математического аппарата. Не имея возможности даже кратко охарактеризовать его, перечислим те главные математические понятия и методы, которые используются в физической геохимии: функция и функциональная зависимость, производная и дифференциалы функций одной и нескольких переменных, их экстремумы, сложные и неявные функции, понятие о полном дифференциале, обыкновенные дифференциальные уравнения и уравнения в частных производных, системы обычных и дифференциальных уравнений и методы их решения с использованием определителей, интегрирование, разложение функций в ряды, понятия векторного анализа. Нетрудно видеть, что эти вопросы не выходят в основном за рамки обычного вузовского курса математики и читатель легко может возобновить его в памяти, подобрав руководство по своим целям и возможностям.
Настоящая глава посвящена термодинамике геологических процессов. Вначале излагаются общеизвестные понятия, законы и положения термодинамики, затем рассматриваются общие вопросы термодинамики природных систем, некоторые важнейшие выводы и соотношения и в заключение - принципы необратимой термодинамики, также в аспекте приложения к природным процессам. Общая особенность главы состоит в том, что термодинамика изложена дедуктивным методом, или, как его обозначают в термодинамике, методом термодинамических потенциалов (методом Гиббса). Преимущества такого метода изложения, отличающегося от общепринятого, существенно индуктивного, очевидны, во всяком случае для наших целей. Прежде всего такое изложение дает возможность строго, с сохранением ясного физического смысла вывести особый термодинамический тип природных систем (здесь мы следуем выводу Д. С. Коржинского). Кроме того, метод термодинамических потенциалов позволяет просто и единообразно получить все общие и частные термодинамические зависимости и уравнения. В настоящей главе мы ограничимся только некоторыми более общими соотношениями, тогда как другие важнейшие термодинамические зависимости перенесены в последующие главы, где они рассматриваются в непосредственном приложении.
Основные понятия
Термодинамическая система определяется как интересующая нас совокупность тел, которую мы противопоставляем внешней среде. Из определения ясно, что не может быть раз и навсегда установленных систем: границы системы каждый раз определяются задачей исследования и физическим содержанием изучаемого явления. Под фазой понимается физически однородная часть системы или совокупность таких тождественных частей, которые ограничены поверхностями раздела, могут быть (в принципе) отделены от других частей системы механическими средствами. Каждый минерал, магма (расплав), газ или жидкий раствор составляют очевидно, особые фазы. Фазы могут иметь постоянный и переменный химический состав. Соотношения между понятиями <фаза> и <минерал> таковы: минерал - твердая фаза, образующаяся в природных условиях. Компонентами системы называются индивидуальные вещества, которые, будучи взяты в наименьшем количестве, достаточны для описания (образования) всех фаз системы. В дальнейшем нетрудно будет убедиться, что выделение компонентов обусловлено конкретным содержанием системы и зависит от тех химических реакций, которые протекают внутри системы и при ее взаимодействии с внешней средой. Отметим еще, что выделение компонентов, хотя и представляется несколько формальной операцией, тем не менее отражает в большинстве случаев более глубокую сущность режима компонентов при формировании систем. В сложных минеральных системах в качестве компонентов обычно выступают окислы или элементы (последние обязательно при окислительно-восстановительных процессах в системах).
Термодинамические системы характеризуются при помощи параметров. Параметрами называются величины, при помощи которых может быть описано состояние системы. Если ограничиться рассмотрением простых термодинамических систем, т. е. таких, в которых происходят только тепловые, механические и химические процессы, то фундаментальными параметрами таких систем будут: температура (Т), энтропия (S), давление (р), объем (V), массы компонентов (ma...mk) и их химические потенциалы (μa...μk).
Экстенсивными называются параметры, обладающие свойством аддитивности (слагаемости), т. е. экстенсивные параметры зависят от массы или числа частиц системы. К экстенсивным параметрам относятся объем, энтропия и массы компонентов. Свойство аддитивности этих параметров очевидно: объем системы равен сумме объемов фаз, масса компонента в системе складывается из масс компонентов в отдельных частях системы и т. д. Экстенсивные параметры иногда называют параметрами емкости. Интенсивными параметрами, или параметрами напряженности, называются такие, которые не зависят от массы или числа частиц системы. К ним относятся температура, давление и химические потенциалы компонентов. Свойство неаддитивности их также очевидно (например, если бы температура обладала свойством аддитивности, то, разбив любую изотермическую систему на бесконечно большое количество частей, мы получили бы бесконечно большую температуру системы, что абсурдно).
Существует примечательное свойство термодинамических параметров, которое можно назвать свойством симметричности и сопряженности. Свойство симметричности состоит в том, что любой термодинамический процесс в системе характеризуется парой параметров, один из которых интенсивный, другой - экстенсивный.
Составим таблицу параметров простых термодинамических систем (табл. 2.1) и рассмотрим процессы, происходящие в таких системах.
| Таблица 2.1. |
| Процессы и параметры | Тепловые | Механические | Химические |
| для компонента а | для компонента b | .... (и так до) | для компонента k |
| Экстенсивные | S | P | ma | mb | ...... | mk |
| Интенсивные | T | V | μa | μb | ...... | μk |
| Уравнение связи (работы) | δQ = TδS | δA = PδV | δWa = μaδma | δWb = μbδmb | ...... | δWk = μkδmk |
Простейшие механические процессы выражаются в изменении объема системы, а причиной изменения объема служит приложенная сила, точнее, сила на единицу площади, равная давлению, оказываемому на систему (или развиваемому системой). Иначе говоря, движущей силой процесса является интенсивный параметр (давление), а выражается процесс в изменении экстенсивного параметра (объема). Элементарная механическая работа в системе будет равна
Приведенное уравнение выражает свойство сопряженности параметров и показывает что при механической работе параметры, ее описывающие (p,V), связаны (сопряжены) уравнением работы.
Тепловые процессы (нагляднее всего перенос тепла в системе) вызываются разностью температуры. При этом в тепловых процессах происходит изменение сопряженного с температурой экстенсивного параметра - энтропии. (В дальнейшем мы несколько подробнее охарактеризуем эту примечательную функцию, здесь же отметим, что под энтропией следует понимать приведенное (т. е. отнесенное к температуре) количество тепла, содержащегося или сообщенного системе, т. е. δS = δQ / T). Соответственно элементарная <тепловая работа>, т. е. количество тепла, полученного или израсходованного системой, выразится соотношением
которое так же, как и (2.1) выражает сопряженность <тепловых> параметров при <тепловой> работе.
При обычных химических процессах происходит изменение количества вещества, или, точнее, масс компонентов в различных частях или фазах системы. Интенсивным параметром и соответственно движущей силой, вызывающей перемещение и вообще изменение количества какого-либо компонента, является химический потенциал этого компонента. Если температура представляет меру <тепловой напряженности> системы и разность температур вызывает перенос тепла (в сторону меньших температур), то аналогично этому химический потенциал выступает как мера <химической напряженности> системы и разность химических потенциалов вызывает перенос вещества (в направлении меньших величин химических потенциалов). Элементарная химическая работа, производимая каким-либо компонентом а, выразится как
Очевидно, что выражение (2.3) справедливо для всех компонентов и суммарная элементарная химическая работа многокомпонентной системы будет равна
 |
(2.4) |
Уравнения (2.3) и (2.4) выражают также как (2.1) и (2.2) свойства сопряженности параметров при <химической работе> компонента a и всех компонентов системы.
Сопоставляя приведенные характеристики различных видов работ простой термодинамической системы, важно отметить следующее. Каждая элементарная работа системы, независимо от ее конкретного вида, может быть представлена как произведение интенсивного параметра (действующей силы Y) на приращение экстенсивного параметра (фактора емкости, или, как говорят координаты процесса δX ); что в обобщенном виде это может быть записано так:
и соответственно
 |
(2.6) |
При этом каждый тип процесса (тепловой, механический, химические) описан парой параметров сопряженных уравнением связи вида (2.5). Отсюда следует что только один из пары сопряженных параметров является независимым (естественно тот который входит под знаком δ). В простой k-компонентной системе, где протекают k+2 процесса, таких независимых параметров оказывается k+2 (ниже это утверждение будет доказано строго). Эти независимые параметры удобно именовать факторами состояния или факторами равновесия.
Заметим, что свойство симметричности и сопряженности присуще любым термодинамическим системам. В сложных термодинамических системах, например с поверхностными, магнитными или электрическими явлениями, каждый процесс будет характеризоваться парой сопряженных параметров - интенсивным и экстенсивным, а элементарная работа выразится произведением действующей силы на изменение фактора емкости или координаты, т. е. уравнением вида (2.5).
Охарактеризуем теперь типы термодинамических систем. В зависимости от внутреннего содержания системы подразделяются: а) по числу компонентов - на однокомпонентные и многокомпонентные (двухкомпонентные, трехкомпонентные и т. д.); б) по числу фаз, из которых состоит система, - на однофазовые, или гомогенные, и многофазовые, или гетерогенные. В зависимости от характера взаимодействия систем с окружающей средой различаются: а) изолированные системы, которые окружены жесткой оболочкой, не пропускающей тепло и вещество; б) закрытые системы, которые могут обмениваться с окружающей средой теплом и работой, но масса их остается постоянной; в) открытые системы, которые могут обмениваться с окружающей средой теплом, работой и слагающими систему компонентами. Кроме того, выделяются различные типы систем по независимым параметрам или факторам равновесия, определяющим поведение системы в тех или иных процессах. Но эти типы систем удобнее рассмотреть позднее, после основных законов термодинамики. Целесообразно также условиться относительно понимания направления изменения систем. Следует различать естественные процессы, как такие изменения систем, которые протекают (или могут протекать) самопроизвольно. Напротив, неестественные процессы не могут осуществляться без внешнего воздействия на систему. Наконец, на границе естественных и неестественных процессов как предельный случай лежат обратимые процессы, т. е. процессы, идущие с одинаковой скоростью в противоположных направлениях.
Первое начало
Термодинамика - наука в основе своей эмпирическая, опирающаяся на многовековой опыт познания природы человеком. Суть ее превосходно выразил А.Эйнштейн: <Термодинамика - это такая наука, которая устанавливает какими должны быть законы природы, чтобы вечный двигатель оказался невозможен>.
В основе термодинамики лежат два главных закона (два принципа или начала), которые показывают какими должны быть законы явлений, чтобы невозможно было возникновение энергии из ничего (вечный двигатель), а именно: 1) закон сохранения энергии и 2) закон рассеяния энергии.
Первое начало - закон сохранения энергии - устанавливает что энергия в системе не исчезает не появляется, а переходит из одной формы в другую. Если мы сообщим системе какое-то количество тепла δQ, то это количество тепла израсходуется на изменение внутреннее энергии системы δU и на работу δA' совершенную системой. Иначе говоря, изменение внутренней энергии системы определяется тем количеством тепла, которое сообщено системе, за вычетом работы, совершенной системой δU = δQ' - δA'.
Поскольку в простой термодинамической системе возможно изменение химической энергии, целесообразно тепло, возникающее в химических реакциях, и химическую работу по переносу вещества выделить из δQ и δA', охарактеризовав их особым членом δW. Член имеет положительный знак, поскольку тепло химических реакций и работа, приводящая к привносу вещества, увеличивают внутреннюю энергию системы1. Тогда получим
Это уравнение представляет полное аналитическое выражение первого начала термодинамики для простой термодинамической системы2, где каждый член δQ, δA и δW характеризует соответственно тепловые, механические и химические процессы в системе.
Изменение внутренней энергии является полным дифференциалом по определению и физическому смыслу как функции состояния системы. Действительно, если бы изменение внутренней энергии не было полным дифференциалом, то значение U могло бы оказаться различным в зависимости от пути перехода системы от одного состояния в другое. Иначе говоря, в зависимости от пути перехода происходило бы появление или исчезновение энергии, а это противоречит первому началу. Это условие в математике кратко обозначается

Напротив, приращения работ δQ, δA и δW не являются полными дифференциалами и, следовательно, количество тепла получаемого (отданного) системой, механическая и химическая работы системы зависят от конкретных форм протекания процесса. Однако и эти процессы можно описать параметрами, обладающими свойствами полного дифференциала. Такие свойства имеют энтропия (S), объем (V), массы компонентов (ma ... m k), являющиеся <приведёнными> работами, т. е. отнесённые к соответствующим интенсивным параметрам:
| dma = δWa / μa ... dmk = δWk / μk |
(2.10) |
(В математике подобная операция называется введением интегрирующего множителя).
Подытоживая сказанное, запишем:
и, подставляя (2.8-2.10), получим окончательное выражение первого начала термодинамики:
 |
(2.12) |
Заметим, что любая работа в определенных условиях может быть произведена таким образом, что она не будет зависеть от пути процесса, а только от начального и конечного состояний системы, т. е. будет функцией состояний системы и соответственно будет обладать свойствами полного дифференциала. Нетрудно видеть, что такие условия, характеризующие максимальную работу системы (подробнее см. ниже), осуществляются: a) dU=dQ при δA=δW=0, б) dU=dA при δQ=δW=0, в) dU = dW при δQ = δА = 0.
Поскольку изменение внутренней энергии представляет полный дифференциал, можно записать

Сопоставляя выражения (2.12) и (2.13), получим важные соотношения

Равенства (2.16), в частности, точно определяют химический потенциал как меру химической напряженности: химический потенциал компонента равен той доле внутренней энергии, которая приходится на единицу массы этого компонента.
Второе начало
Если первое начало термодинамики характеризует условия протекания процессов, то второе - устанавливает направленность процессов. Второе начало термодинамики - закон рассеяния энергии - можно в общем виде сформулировать так: существует такая функция состояния системы, называемая энтропией (S), которая возрастает при всех естественных процессах. Эта зависимость записывается так:
Заметим, что в термодинамической литературе известно около двух десятков различных формулировок второго начала. Существует также стремление разделить его на два самостоятельных принципа. Один принцип устанавливает существование энтропии: имеется такая функция состояния S, называемая энтропией, которая определяется как dS = δQ / T (2.17a) и S = Σ(δQ / T) = Q / T (2.17б) (что, вообще говоря, далеко не элементарно), и второй - определяет возрастание энтропии при всех естественных процессах:
Однако для наших целей можно ограничиться обобщенным началом в приведенной формулировке, которая кажется предпочтительней из других возможных определений второго начала. Физический смысл второго начала обычно иллюстрируется образным примером переноса тепла. Пусть две фазы или части системы (обозначим их индексами A и B) находятся при разной температуре, причем TA > TB. В таких условиях естественным будет процесс переноса тепла от более нагретого тела A к менее нагретому B. Пусть при этом будет перенесено некоторое количество тепла Q'. Тогда  , в справедливости чего легко убедиться: поскольку TA > TB, а количество тепла одно и тоже. Согласно определению энтропии (2.17) , в справедливости чего легко убедиться: поскольку TA > TB, а количество тепла одно и тоже. Согласно определению энтропии (2.17)  , тогда в этом и в любом другом естественном процессе ΔS = SB - SA > 0 - энтропия системы будет возрастать. Можно напомнить, что когда впервые Р. Клаузиус ввел понятие энтропии, второе начало термодинамики было изложено им так: <Не может происходить самопроизвольная передача тепла от холодного тела к более горячему>. , тогда в этом и в любом другом естественном процессе ΔS = SB - SA > 0 - энтропия системы будет возрастать. Можно напомнить, что когда впервые Р. Клаузиус ввел понятие энтропии, второе начало термодинамики было изложено им так: <Не может происходить самопроизвольная передача тепла от холодного тела к более горячему>.
Таким образом, второе начало термодинамики устанавливает направленность процессов: все естественные процессы протекают с возрастанием энтропии: dS > δQ / T, все неестественные, напротив, с уменьшением энтропии dS < δQ / T, и предельный тип обратимых процессов осуществляется в условиях dS = δQ / T.
Если обозначить изменения тепла и энтропии в обратимом процессе индексом е, то второе начало можно представить в следующем виде:

где δQi - количество тепла, связанного (рассеянного) системой в любом естественном процессе, dSi - соответствующее ему возрастание энтропии. Член δQi носит название некомпенсированного тепла, он характеризует ту долю тепла, которая теряется в любом естественном процессе и не может быть превращена в полезную работу системы. Это, собственно, равнозначное определение второго начала, оно отражается в известных формулировках: <Невозможен процесс, имеющий единственным своим результатом превращение тепла в работу>, или <двигатель второго рода (т. е. превращающий все тепло в работу) невозможен> (Оствальд, Планк и др.). Следует заметить, что второе начало, как и первое, в рамках феноменологической термодинамики постулируется. Безупречное обоснование второго начала возможно, пожалуй, только методами статистической термодинамики. Рассмотрение этих вопросов выходит далеко за рамки наших задач, поэтому ограничимся самыми краткими сведениями. Статистическое содержание энтропии и второго начала вскрывается известными формулами Л. Больцмана:
| ΔS = S2 - S1 = k ln (w2/w1) |
(2.20) |
где k - постоянная Больцмана (равная R/N), a w - термодинамическая вероятность состояния системы. Согласно (2.19) и (2.20), энтропия выступает как мера термодинамической вероятности данного состояния системы, а возрастание энтропии отражает переход системы из термодинамически менее вероятного в более вероятное состояние. <Природа стремится от состояний менее вероятных к более вероятным> - формулировка второго начала, данная Л. Больцманом. Следует пояснить, что термодинамическая вероятность отличается от математического понимания вероятности. Если в математике вероятность выражает отношение числа благоприятных случаев, событий или состояний к их общему числу (т. е. математическая вероятность всегда меньше единицы), то термодинамическая вероятность представляет число способов (точнее, микросостояний), которыми может быть осуществлено данное состояние систем (т. е. термодинамическая вероятность всегда больше единицы). Рассматривая статистическими методами распределение частиц в системе, можно показать, что чем большим числом способов можно осуществить данное состояние, тем более вероятным оно является и соответственно отвечает максимуму энтропии системы. Отметим также, что статистический смысл энтропии и других термодинамических параметров имеет важнейшее значение для их вычисления.
Условия равновесия
Из второго начала термодинамики непосредственно вытекают условия равновесия термодинамических систем. Рассмотрим сначала изолированную систему. Все естественные процессы в такой системе будут приводить к возрастанию энтропии при сохранении неизменной (в силу условий существования изолированной системы) внутренней энергии системы. Тогда, очевидно, термодинамическая система находится в равновесии, если при данной (постоянной) внутренней энергии энтропия системы максимальна, т. е. при
| U = const, S=max, dS=0, d2S < 0.
|
(2.21) |
Как было впервые показано В. Гиббсом, сформулированному критерию равновесия полностью эквивалентен другой критерий: термодинамическая система находится в равновесии, если при данной (постоянной) энтропии внутренняя энергия системы минимальна, т. е. при
| S = const.
U = min, dU = 0 d2U > 0.
|
(2.22) |

Наглядное графическое изображение доказательства теоремы Гиббса приводит в своей монографии Д. С. Коржинский.
Пусть мы имеем равновесное состояние системы с SI и UI (рис. 2.1) где SI=max. Допустим, что этому состоянию SI может отвечать другое состояние системы с еще меньшей энергией (точка SIUII ), но тогда чтобы повысить энергию системы до UI мы должны сообщить системе тепло, что приведет к увеличению ее энтропии до SII (точка SIIUI). Иначе говоря если возможно состояние SIUII , то обязательно возможно состояние SIIUI. Но это противоречит условию SI=max и следовательно возможно одно единственное соотношение: если S=max (при U=const), то U=mIn (при S=const).
Разберем условия равновесия термодинамических систем несколько подробнее. Максимум энтропии как критерий равновесия характеризует изолированную систему, которая окружена жесткой оболочкой (V=const), не пропускающей тепло (U=const) и вещество  , т. е. S = ƒ (U, V, ma ... mk). Изолированные системы в природе не встречаются и представляют термодинамическую абстракцию. Минимум внутренней энергии как критерий равновесия относится уже к другой системе, называемой изохоро-изоэнтропической, которая характеризуется постоянством энтропии объема и масс компонентов, т. е. U = ƒ (S, V, ma ... mk). Нетрудно представить, что те естественные процессы, которые в изолированной системе приводили к возрастанию энтропии, в этой системе могут осуществляться только путем отвода тепла от системы (так как энтропия ее постоянна), что вызывает уменьшение внутренней энергии системы. В соответствии с первым и вторым началами выражение внутренней энергии гомогенной, однофазовой системы в состоянии равновесия имеет вид , т. е. S = ƒ (U, V, ma ... mk). Изолированные системы в природе не встречаются и представляют термодинамическую абстракцию. Минимум внутренней энергии как критерий равновесия относится уже к другой системе, называемой изохоро-изоэнтропической, которая характеризуется постоянством энтропии объема и масс компонентов, т. е. U = ƒ (S, V, ma ... mk). Нетрудно представить, что те естественные процессы, которые в изолированной системе приводили к возрастанию энтропии, в этой системе могут осуществляться только путем отвода тепла от системы (так как энтропия ее постоянна), что вызывает уменьшение внутренней энергии системы. В соответствии с первым и вторым началами выражение внутренней энергии гомогенной, однофазовой системы в состоянии равновесия имеет вид
 |
(2.12) |
Кроме этого уравнения, поскольку dU является полным дифференциалом, справедливы соотношения (2.14, 2.15, 2.16):

Таким образом, в состоянии равновесия 2k+5 параметров, входящих в уравнение (2.12), связаны k+3 уравнениями: одно уравнение (2.12) и k+2 уравнения (2.14)-(2.16). Это означает что число независимых параметров или факторов состояния в однофазовой системе равно f= (2k+5)-(k+3) =k+2 параметра. Факторами состояния рассматриваемой системы являются S, V, ma...mk, и если при определенном (постоянном) значении их внутренняя энергия как функция факторов состояния имеет минимальное значение, система находится в равновесии.
Обратимся теперь к гетерогенной, многофазовой, изохоро-изоэнтропической системе. Изменение внутренней энергии такой системы выразится, очевидно, как сумма изменений внутренней энергии всех фаз системы от А до R, число которых равно r, т. е. как сумма r уравнений вида (2.12):

Причем, согласно определению системы (S, V, ma...mk=const): т. е.

Выполнение условия равновесия системы U=min, или dU=0, d2U>0 возможно только при таком состоянии системы, когда интенсивные параметры во всех фазах равны, т. е. при условии

В справедливости уравнений (2.24) легко убедиться. Пусть температуры двух фаз или частей системы не равны, например ТА > ТВ. Тогда в системе, очевидно, будет происходить естественный процесс переноса тепла от более нагретой фазы -δQA = -TAdS к менее нагретой +δQB = TBdS, который приведет к уменьшению внутренней энергии системы: dU = -TAdS + TBdS = (TB-TA)dS < 0. Иначе говоря, минимальное значение внутренней энергии системы будет достигнуто в таком состоянии, когда температура во всех фазах или частях системы станет одинаковой. Обратим внимание, что по мере достижения равновесия система будет совершать <тепловую работу> (отдавать тепло) и эта работа будет максимальной (поскольку dU-полный дифференциал).
Точно так же пусть, например, давление в одной фазе или части системы (А) будет больше давления в другой фазе (В): рА > рВ. В этом случае будет происходить увеличение объема первой фазы (+pАdV) за счет уменьшения объема второй фазы (-pВBdV), в результате чего внутренняя энергия системы будет уменьшаться: dU=-(рАdV-pВdV)=(pВ-рА)dV < 0. Ясно, что уменьшение внутренней энергии за счет механической работы будет продолжаться до тех пор, пока давление во всех фазах или частях системы не станет одинаковым, и это уменьшение внутренней энергии будет отражать максимальную механическую работу системы.
Наконец, аналогичным образом легко показать, что если химический потенциал какого-либо компонента в одной фазе больше, чем в другой, например μAa > μBa, то компонент из фазы с большим химическим потенциалом будет переходить в фазу с меньшим химическим потенциалом, а это приведет к уменьшению внутренней энергии cистемы: dU = -μAadma + μBadma = (μBa-μAa)dma < 0. Очевидно также, что равенство химических потенциалов компонентов по фазам отвечает минимальному значению внутренней энергии системы, или, что то же, состоянию равновесия, а уменьшение внутренней энергии при достижении равновесия выражает максимальную химическую работу системы.
Таким образом, уравнения (2.24) определяют необходимые условия равновесия гетерогенной, многофазовой, многокомпонентной системы. Их можно сформулировать так: для того чтобы гетерогенная термодинамическая система находилась в состоянии равновесия необходимо, чтобы интенсивные параметры во всех фазах системы были равны. Обратим внимание на то, что это условие является необходимым, но недостаточным критерием равновесия. Возможны такие состояния системы, когда интенсивные параметры по всем фазам системы равны, но внутренняя энергия не является минимальной, т. е. в системе, в принципе, осуществимы такие преобразования, которые при данных значениях интенсивных параметров приведут к уменьшению внутренней энергии системы. Такие состояния системы называются метастабильными. Метастабильные состояния очень широко распространены в природных минеральных системах, когда минеральные фазы и ассоциации, образованные при высоких температурах и давлениях, сохраняются при низких температурах и давлениях, например на поверхности Земли. Причина устойчивости метастабильных состояний - кинетическая, её следует рассматривать уже c позиций кинетики, а не термодинамики.
В отличие от метастабильных, полностью равновесное состояние, отвечающее минимальной внутренней энергии при данных значениях факторов состояния, обозначается как стабильное. Таким образом, равенство по фазам интенсивных параметров - дополнительное необходимое условие равновесия многофазовых систем, вытекающее для гетерогенных систем из единственного необходимого и достаточного признака равновесия - минимума внутренней энергии (или максимума энтропии) при определенных (постоянных) значениях факторов состояния системы.
Рассмотрим теперь вопрос о числе независимых параметров или факторов состояния в многофазовых системах. Как было показано, однофазовая система в состоянии равновесия определяется k+2 независимыми параметрами. В гетерогенной системе, состоящей из r фаз, возможное число независимых параметров (k+2)r ограничено условиями равновесия (2.24), т.е. (k+2)(r-1) уравнениями. Тогда число независимых параметров равно: ƒ = (k+2)r - (k+2)(r-1) = k+2. Таким образом, состояние равновесной гетерогенной системы полностью определяется k+2 независимыми параметрами, или факторами состояния. Физическое содержание этого вывода легко пояснить, обратившись к табл.2.1: если система находится в равновесии, т. е. U=min, dU=0, то каждая пара параметров, характеризующих различные виды работ системы, сопряжена уравнением связи таким образом, что только k+2 из них (по одному на каждый вид работ) могут изменяться независимо, т. е. являться факторами состояния. Независимыми параметрами изохоро-изоэнтропической системы, функция факторов состояния, или просто функция состояния, которой - внутренняя энергия, являются энтропия, объем и массы компонентов (они входят под знаком дифференциала в уравнения 2.12 и 2.23).
Термодинамические потенциалы
Продолжим рассмотрение внутренней энергии как функции состояния изохоро-изоэнтропической системы. Поскольку в условиях равновесия значения интенсивных параметров одинаковы во всех фазах системы, то уравнение (2.23) для равновесных состояний может быть равносильно заменено уравнением (2.12):
 |
(2.12) |
которое справедливо и для гомогенных, и для гетерогенных равновесных систем. Приведем еще одно самое общее выражение изменения внутренней энергии, где в развернутой форме через факторы состояния выражено равновесное значение dU, а членом δQi - некомпенсированное тепло - суммарно обозначены необратимые изменения dU по мере достижения равновесия:
 |
(2.25) |
Если система находится в равновесии δQi = 0 и интенсивные параметры равны во всех частях и в системе в целом, то уравнение изменения внутренней энергии (2.12) можно интегрировать, принимая, что интенсивные параметры не зависят от сопряженных экстенсивных. В результате получим
Проведенное интегрирование равносильно увеличению размера и соответственно экстенсивных параметров системы: удвоению, утроению размеров ее части, переходу от части к целому, от бесконечно малых к конечным. Очевидно, что при этой операции в равновесной системе T, P, μa...μk могут рассматриваться как постоянные множители, а U0 представляет константу интегрирования, зависящую от начального состояния системы, и если принять его бесконечно малым по размерам и с ничтожным теплосодержанием, то U0 ~= 0. В дальнейшем изложении, как и принято в курсах термодинамики, эта константа опущена и использовано следующее выражение интегральной внутренней энергии:
 |
(2.26) |
Подведем некоторые итоги рассмотрения свойств внутренней энергии. Выше было показано, что внутренняя энергия: а) является функцией состояния системы и ее дифференциал обладает свойствами полного дифференциала, б) становится минимальной в состоянии равновесия, в) представляет собой характеристическую функцию в том смысле, что производные этой функции по термодинамическим параметрам тоже являются термодинамическими параметрами; г) изменение внутренней энергии равно максимальной работе, которую совершает система по мере достижения состояния равновесия. Функции, характеризующиеся совокупностью отмеченных свойств, являются в термодинамике фундаментальными и носят специальное название - термодинамические потенциалы. Приведем определение: термодинамическим потенциалом называется характеристическая функция состояния системы, которая убывает при всех необратимых процессах, производя при этом максимальную работу, и становится минимальной в состоянии равновесия. Следовательно, внутренняя энергия представляет таким образом, термодинамический потенциал изохоро-изоэнтропической системы.
Выведем теперь термодинамические потенциалы других типов систем, различающихся по набору факторов состояния, или, что то же, по характеру взаимодействия их с окружающей средой. Ограничимся возможными вариациями факторов состояния, характеризующих только тепловые и механические процессы. Обратившись к табл. 2.1, нетрудно видеть, что кроме рассмотренной системы S, V, ma...mk в силу сопряженности параметров можно предполагать существование только таких систем: T, V, ma...mk; S, p, ma...mk; T, p, ma...mk. Каждая из этих систем отличается от изохоро-изоэнтропической системы заменой одного или двух экстенсивных параметров, характеризующих тепловые и механические процессы, на сопряженные интенсивные параметры. Всё эти типы систем имеют реальное содержание, встречаются в природе и производственной практике и этим прежде всего определяется целесообразность выявления особенностей систем, условия существования которых выражаются заменой экстенсивных факторов состояния на сопряженные интенсивные. Рассмотрим кратко физический смысл различных условий существования систем и выведем их характеристические функции - термодинамические потенциалы.
Обратимся сначала к изохро-изотермической системе с факторами состояния T, V, ma...mk. В отличие от изохоро-изоэнтропической в рассматриваемой системе фактором состояния, регулирующим тепловые процессы, служит температура, определяемая внешней по отношению к системе средой. Одинаковая температура для всех частей этой системы устанавливается не в результате достижения равновесия (как это было в изоэнтропической системе), а предопределена заранее и всегда обеспечивается физическими условиями существования системы. Следовательно, уменьшение термодинамического потенциала в системе не может происходить за счет выравнивания температур, и система не может производить <тепловую работу>. Тогда для того, чтобы получить из внутренней энергии значение термодинамического потенциала изохоро-изотермической системы, мы должны каким-то образом удалить (вычесть) из внутренней энергии (уравнение 2.26) член, характеризующий тепловую работу системы. Соответствующее корректное математическое преобразование замены одного параметра на сопряженный носит название <преобразования Лежандра>, смысл его ясен из нижеследующего.
Термодинамический потенциал изохоро-изотермической системы (в учебниках термодинамики ее обычно обозначают сокращенно как изотермическую), называемый свободной энергией Гельмгольца, или просто свободной энергией F=ƒ(T,V,ma...mk), равен:

Условия равновесия изохоро-изотермической системы F = ƒ(T, V, ma...mk) = min, dF = 0 и d2F > 0, что непосредственно следует из уравнения (2.28). Легко показать, что для равновесной гетерогенной изохоро-изотермической системы необходимо также равенство по фазам давлений и химических потенциалов компонентов 3. Наконец, уменьшение свободной энергии по мере достижения равновесия (-δQi=dF< 0) представляет максимальную (dF-полный дифференциал) полезную работу системы, слагающуюся из собственно механической работы расширения и работы вследствие химических процессов в системе.
Рассмотрим теперь изобаро-изоэнтропическую систему с факторами cостояния S, p, ma...mk, которая характеризуется равенством давления во всех частях системы, предопределенным условиями существования системы. Термодинамический потенциал такой системы, рассуждая аналогично вышеизложенному, может быть получен путем вычитания из внутренней энергии члена, характеризующего механическую работу системы. Распространяя, таким образом, преобразование Лежандра на член - pV, получим выражение термодинамического потенциала изобаро-изоэнтропической системы (ее обозначают часто как изобарическую), который носит название энтальпии H = ƒ(S, p, ma...mk):

 |
(2.30) |
Условием равновесия изобаро-изоэнтропической системы является минимум энтальпии: H = ƒ (S, p, ma...mk) = min или dH = 0, d2H > 0. Для этого в гетерогенной системе необходимо равенство по фазам температур и химических потенциалов компонентов, что может быть показано аналогично рассмотренному выше (в примечаниях) для F-потенциала. Факторы состояния ƒin + ƒex = 1 + (k+1) = k + 2. Изменение энтальпии dH является полным дифференциалом и уменьшение H-потенциала по мере приближения к состоянию равновесия будет характеризовать максимальную теплоотдачу системы: -δQi = dH < 0. Поскольку H-система не может производить механическую работу, уменьшение термодинамического потенциала происходит только путем отдачи тепла системой. За эти свойства энтальпию нередко называют теплосодержанием.
Наконец, изотермо-изобарические системы характеризуются факторами состояния: G = ƒ (T, p, ma...mk). В этих системах равенство по фазам температур и давлений задано условиями существования системы, и, уменьшение термодинамического потенциала (полезная работа системы) не может происходить за счет их выравнивания внутри системы. Тогда, вычитая из внутренней энергии члены соответственно тепловой (TS) и механический (pV) работы, получим выражение термодинамического потенциала изотермо-изобарической системы, который носит название свободной энергии Гиббса, потенциала Гиббса, изотермо-изобарического потенциала или собственно термодинамического потенциала:
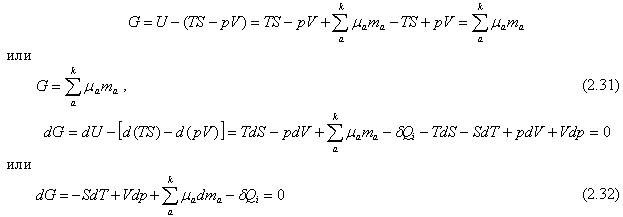
Очевидно, что аналогично рассмотренному выше условием равновесия изотермо-изобарический системы является минимум термодинамического потенциала: G = ƒ (T, p, ma...mk) = min, dG = 0 и d2G>0 для чего в гетерогенной системе должно выполняться условие равенства химических потенциалов по всем фазам. Факторы состояния ƒin + ƒex = 2 + k = k + 2 (ƒin = T, ƒex = ma...mk). Функция dG является полным дифференциалом и изменение свободной энергии Гиббса (G-потенциала) характеризует максимальную работу химических процессов, поскольку система не может производить ни механической работы, ни передачи тепла.
Сопоставляя уравнения (2.26), (2.27), (2.29) и (2.23), можно получить соотношения между четырьмя основными характеристическими функциями:
| G = U - TS - (-pV) = H - TS = F - (-pV) |
(2.33) |
где, очевидно, F=U-TS и H=U+pV.

Все термодинамические потенциалы являются экстенсивными параметрами и имеют размерность энергии (так же, как и каждое произведение интенсивного параметра на соответствующий экстенсивный). Функции Н и U носят в термодинамике названия тепловых функций (что по отношению к U недостаточно, так как в равной мере U отражает и работу системы). Из соотношения H=U+pV следует что δQp > δQV (где δQp=δH и δQV=δU), т. е. тепло, полученное (отданное) системой в изобарических условиях, всегда больше изохорического теплового эффекта. Из соотношения F=U-TS следует уже обсуждавшееся выше заключение о том, что максимальная полезная работа системы всегда меньше ее внутренней энергии, часть которой в системе T, V, m идет на возрастание энтропии системы (из выражения (2.28) можно убедиться, что увеличение S уменьшает F). Максимальная полезная работа изотермической системы складывается из собственно работы расширения δАV и работы химических процессов в системе δАW, которые имеют как уже отмечалось, разные знаки, т.е. δАT = - dF = δАV - δАW. Свободная энергия Гиббса G характеризует химическую энергию системы. Изменение G отражает тепловые и объемные эффекты химических процессов в системе, которые протекают (при данных Т и р) в направлении увеличения энтропии и уменьшения объема системы (что, согласно выражению (2.32), приведет к уменьшению G). Сопоставление G=F+pV=Н-TS показывает что химическая энергия системы также не может быть полностью реализована в виде полезной работы, часть ее обязательно будет рассеяна, т. е. израсходована на возрастание энтропии системы.
Рассмотренные соотношения между термодинамическими потенциалами графически изображены в верхней части рис.2.2. В нижней части показаны экстремальные значения (максимум и минимум) факторов состояния (они соединены линиями) и сопряженных параметров (показали стрелками) в условиях равновесия и максимальной работы для каждого типа систем. Доказательства соответствующих экстремумов непосредственно следуют из уравнений термодинамических потенциалов и легко могут быть выражены, используя их свойства полных дифференциалов, через частные производные по факторам состояния. Так, для U = ƒ (S, V, m):  и минимальному значению U будет отвечать минимум T и максимум p. Для системы G = ƒ (T, p, m), и минимальному значению U будет отвечать минимум T и максимум p. Для системы G = ƒ (T, p, m),  и минимальному значению свободной энергии G будет отвечать максимум S и минимум p, и аналогично для всех систем. Свойство термодинамических потенциалов как полных дифференциалов широко используется в термодинамике для анализа самых разнообразных термодинамических зависимостей. и минимальному значению свободной энергии G будет отвечать максимум S и минимум p, и аналогично для всех систем. Свойство термодинамических потенциалов как полных дифференциалов широко используется в термодинамике для анализа самых разнообразных термодинамических зависимостей.
Рассмотренные термодинамические потенциалы как характеристические функции состояния систем были выведены во второй половине прошлого века Ф. Массье и Дж. Гиббсом, а принятый нами метод изложения от исходных начал термодинамики через термодинамические потенциалы как общие функции состояния и далее к частным выводам обозначается обычно как метод Гиббса, поскольку им впервые термодинамика была изложена дедуктивно в самом общем виде. Этот метод изложения, к сожалению, не получил широкого признания, по-видимому, в основном потому, что соответствующие математические выводы не сопровождались достаточным истолкованием физического смысла операций. Термодинамика по-прежнему излагается как совокупность множества эмпирических соотношений, хотя в конце всех полных курсов приводится характеристика метода Гиббса (Герасимов и др., 1963; Базаров, 1961; и др.). В полной мере метод Гиббса использован только в работах Э. Гугенгейма (1941, 1950), В. Шоттки и др. (Schottky et а1., 1929) и Д. С. Коржинского (1957, 1972), в какой-то мере в курсе А. Мюгстера (1971). Мы сознательно следовали в выводе термодинамических потенциалов ближе всего изложению Д. С. Коржинского, опустив при этом подробные математические выкладки и еще более усилив рассмотрение физического смысла операций.
Общие критерии равновесия и термодинамические потенциалы, число независимых параметров и правило фаз
Обратимся еще раз, на новом уровне, к обсуждению условий равновесия термодинамических систем. Можно сформулировать следующее самое общее положение: термодинамическая система находится в равновесии, если при данных определенных факторах состояния термодинамический потенциал ее имеет минимальное значение, или, короче, - необходимым и достаточным условием равновесия любой термодинамической системы является минимум ее термодинамического потенциала, т. е.
| Ф=min, dФ=0, d2Ф>0. |
(2.34) |
Как было показано выше, выполнение этого условия в гетерогенной системе требует равенства интенсивных параметров по всем фазам системы. Наконец, из этого условия обязательно следует что если система находится в равновесии, то ее состояние полностью характеризуется k+2 независимыми параметрами, которые, как отмечалось, обычно называют факторами состояния, или факторами равновесия. Указанные положения были доказаны для изохоро-изоэнтропической системы, но они полностью распространяются и на все другие типы систем. Правомерность этого непосредственно следует из тех ограничений, которые наложены на условия существования других рассмотренных типов систем и может быть строго доказана для каждой системы независимо.
Представление о термодинамическом равновесии относится к фундаментальным понятиям термодинамики, и правильное понимание его как бы предопределяет возможности использования термодинамических методов. В связи с этим необходимо обсудить еще несколько вопросов.
Во многих курсах термодинамики при выводе термодинамических потенциалов используется представление о закрытых системах, т.е. априори принимается dma=dmb=...=dmk=0 и термодинамические потенциалы рассматриваются без члена, характеризующего химическую энергию (например, dU=TdS-PdV, dH=dU+d(pV)=TdS+Vdp и т. д.). Строго говоря, это, конечно, неправильно, поскольку выражение химической энергии компонентов входит во все термодинамические потенциалы и уменьшение термодинамического потенциала вследствие уменьшения химической энергии может происходить во всех системах, в том числе и в закрытых, которые не обмениваются компонентами с окружающей средой.
Общепринято также рассматривать условия равновесия применительно к изолированным и затем к закрытым системам. Однако критерии равновесия никак не связаны с условиями изоляции систем от окружающей среды. Поясним это следующим логическим опытом. Выделим в пределах равновесной системы (система А) какую-либо часть ее (новая система В), также, естественно, находящуюся в состоянии равновесия. Если систему В заключить в непроницаемую для вещества оболочку, то состояние системы от этого никак не изменится, она будет продолжать находиться в равновесии, так как условие  входит в определение равновесной системы. Если же система В, заключенная в непроницаемую для вещества оболочку, находится в состоянии равновесия и в равновесии с системой А (т. е. при тех же значениях интенсивных параметров), то состояние ее не изменится, если снять изолирующую оболочку, так как при данных значениях факторов состояния равновесное состояние является единственно стабильным, поскольку характеризуется минимальным значением термодинамического потенциала. Таким образом, сформулированные условия равновесия полностью распространяются и на открытые системы, на что было указано еще Д. Гиббсом. Более того, как увидим ниже, условия той или иной изоляции накладывают дополнительные ограничения на системы, никоим образом не вытекающие из критериев равновесия, которые справедливы для всех систем, в том числе и для открытых систем. входит в определение равновесной системы. Если же система В, заключенная в непроницаемую для вещества оболочку, находится в состоянии равновесия и в равновесии с системой А (т. е. при тех же значениях интенсивных параметров), то состояние ее не изменится, если снять изолирующую оболочку, так как при данных значениях факторов состояния равновесное состояние является единственно стабильным, поскольку характеризуется минимальным значением термодинамического потенциала. Таким образом, сформулированные условия равновесия полностью распространяются и на открытые системы, на что было указано еще Д. Гиббсом. Более того, как увидим ниже, условия той или иной изоляции накладывают дополнительные ограничения на системы, никоим образом не вытекающие из критериев равновесия, которые справедливы для всех систем, в том числе и для открытых систем.
Еще одно очень существенное дополнение. При рассмотрении состояния равновесия было принято, что факторы состояния систем являются постоянными. Этот традиционный в термодинамике подход увековечен названиями систем: изотермическая, изобарическая и т. д. (где приставка <изо> по-гречески означает постоянный). Такой прием дает возможность установить и охарактеризовать условия равновесия наиболее простым и ясным способом. Однако выявив таким образом признаки и критерии равновесия, можно показать, что постоянство факторов состояния не является обязательным условием равновесия. Действительно, пусть k+2 независимых параметров, определяющих состояние системы, не являются постоянными, а находятся в процессе изменения. Пусть при этом процессы в системе осуществляются таким образом, что в каждый данный момент все другие параметры системы полностью определяются k+2 факторами состояния, а термодинамический потенциал как функция факторов состояния в каждый данный момент имеет минимальное значение. Очевидно, что состояние такой системы в каждый данный момент будет полностью равновесным, поскольку нет и не может быть какого-либо другого равновесного состояния системы, кроме того, которое характеризуется минимумом термодинамического потенциала системы. Такое поведение систем имеет определенный физический смысл. Оно означает что изменение зависимых параметров системы должно происходить быстрее, чем меняются факторы состояния системы. Например, в системе, получающей тепло от окружающей среды (фактор состояния - энтропия), распространение тепла должно осуществляться с такой скоростью, что (в пределах интересующей нас точности) вся система в каждый данный момент должна находиться при одинаковой температуре. Или, например, изменение объема системы должно происходить таким образом, чтобы давление в каждый данный момент было равно во всех частях системы. Нетрудно убедиться, что осуществление равновесных систем с изменяющимися факторами состояния определяется физическим содержанием протекающих при этом процессов и зависит также от степени детальности и точности, с которой мы подходим к описанию системы. Таким образом, состояние термодинамического равновесия характеризует определенную взаимосвязь параметров, при которой все термодинамические параметры системы являются функцией k+2 факторов состояния и каждому значению факторов состояния отвечает минимум термодинамического потенциала системы, независимо от того, изменяются факторы состояния или остаются постоянными.
Представление о термодинамическом равновесии как о взаимосвязи параметров изменяющихся систем имеет принципиальное методологическое значение в термодинамике. Оно было выдвинуто Д. С. Коржинским (1957) в противовес общепринятому толкованию равновесия как состояния полного покоя системы, в которой все естественные процессы прошли и которая не претерпевает каких-либо изменений. Такие <мертвые> состояния, не встречаются в природе, а составляют искусственную абстракцию, применимость которой к анализу природных процессов неоднократно подвергалась сомнению. Рассмотренное представление о равновесии как об определенной взаимосвязи параметров снимает с понятия равновесия незаслуженные <методологические оковы>, показывает его главную идейную сущность и открывает широкие возможности использования термодинамических методов при анализе природных явлений. Как отмечалось выше, одна из главнейших особенностей природных процессов состоит как раз в том, что они осуществляются в условиях мозаичного или локального равновесия, когда при общем необратимом изменении систем и факторов состояния в каждый данный момент в каждом данном участке достигается состояние равновесия.
Следует заметить, что тенденция распространения понятий и методов равновесной термодинамики на изменяющиеся системы присуща и классической термодинамике, особенно в последнее время в связи с развитием неравновесной термодинамики. Это находит свое отражение в появлении представлений о <квазиравновесных>, или <квазистатических>, процессах (Герасимов, 1963; А. Самойлович, 1955; К. Путилов, 1965) или, в более явной форме, во введении понятия локального равновесия (Базаров, 1961).
Обратим внимание на две важные стороны выражения термодинамической работы через термодинамические потенциалы систем. Возьмем, для конкретности, изотермо-изобарическую систему G = ƒ (T, p, ma...mk). Выражение ее термодинамического потенциала в дифференциальной форме, как было показано выше
 |
(2.32) |
При достижении равновесия, при постоянных факторах состояния системы (dT = 0, dp = 0,  ) внутри ее происходит выравнивание химических потенциалов компонентов по фазам и полезная работа системы приводит к уменьшению ее свободной энергии вплоть до состояния равновесия (δQi), когда G = min и dG = 0: ) внутри ее происходит выравнивание химических потенциалов компонентов по фазам и полезная работа системы приводит к уменьшению ее свободной энергии вплоть до состояния равновесия (δQi), когда G = min и dG = 0:
 |
(2.32) |
Иной характер имеет изменение G-потенциала при изменении факторов состояния системы. Как можно видеть из уравнения (2.32) при повышении температуры (+dT) G-потенциал уменьшается (dGP,m = -SdT), а при увеличении давления (+dp) - напротив, увеличивается (dGT,m = Vdp). При увеличении масс компонентов (+Σdm) свободная энергия тоже увеличивается ( ), но это увеличение будет минимальным, так как внутри системы будут протекать быстрые релаксирующие процессы выравнивания химических потенциалов компонентов по фазам, уменьшающие G-потенциал. ), но это увеличение будет минимальным, так как внутри системы будут протекать быстрые релаксирующие процессы выравнивания химических потенциалов компонентов по фазам, уменьшающие G-потенциал.
Аналогичным образом можно рассмотреть изменения термодинамических потенциалов (U, F, H) других систем. Вывод из изложенного очевиден: термодинамические потенциалы как функции состояния описывают две различные стороны поведения систем - <внешнюю>, вызванную изменением факторов состояния (при этом термодинамические потенциалы могут и возрастать и уменьшаться) и <внутреннюю> (когда термодинамические потенциалы всегда уменьшаются в приближении к состоянию равновесия).
Рассмотрим теперь в самом общем виде соотношение между числом интенсивных и экстенсивных параметров равновесных систем. Общее число независимых параметров равновесной системы, как было показано, равно:
Определим число экстенсивных параметров. Обратимся сначала к равновесной гомогенной изохоро-изоэнтропической системе, состояние которой также определяется k+2 независимыми параметрами.
Уравнения состояния системы:
 |
(2.26) |
и
 |
(2.12) |
Дифференцируя первое уравнение по всем параметрам и сравнивая с ним (вычитая) второе уравнение, получим следующее выражение, известное как уравнение Гиббса-Дюгема:
 |
(2.36) |
Нетрудно убедиться, что такое же выражение будет получено при рассмотрении любой другой термодинамической системы; например, для изотермо-изобарической системы, где  , дифференцируя это выражение по обоим параметрам , дифференцируя это выражение по обоим параметрам  и, вычитая это выражение из и, вычитая это выражение из  , получим уравнение (2.36): , получим уравнение (2.36):
 |
(2.36) |
Уравнение Гиббса-Дюгема содержит дополнительную характеристику равновесных термодинамических систем. Оно показывает существование зависимости между интенсивными параметрами системы. Следовательно, из k+2 параметров гомогенной системы по крайней мере один, вследствие уравнения связи (2.36), должен быть экстенсивным (например, масса или объем фазы). Физическое содержание этого заключения очевидно: не может, конечно, существовать систем или фаз, заданных только одними интенсивными параметрами - такие системы нематериальны.
Гетерогенная система, состоящая из r фаз, должна содержать, по крайней мере r экстенсивных параметров, так как каждая фаза должна быть задана в силу уравнения (2.36) одним экстенсивным параметром:
Тогда, сопоставляя выражение (2.37) с уравнением (2.35), видим, что ƒin = k + 2 - ƒex = k + 2 - r и, обозначая ƒin = n, получим выражение
Это уравнение представляет одну из фундаментальных зависимостей термодинамики - правило фаз Гиббса. Правило фаз Гиббса. устанавливает соотношение между числом независимых интенсивных параметров, или числом степеней свобод (n), числом фаз и числом компонентов в системе. Оно показывает каково максимальное число независимых интенсивных параметров, совместимое с данным фазовым составом данной k-компонентной системы. Правило фаз имеет широкое приложение в термодинамике, особенно в физико-химическом анализе.
Формула правила фаз может быть выведена различными способами. Покажем еще один - наиболее часто встречающийся. Поскольку максимальное число интенсивных параметров, характеризующих одну фазу, равно k+1, то в системе из r фаз возможно (k+1)r интенсивных параметров. Однако эти интенсивные параметры в равновесной системе связаны как мы видели (k+2)(r-1) уравнениями равенства параметров по фазам (уравнения 2.24). Тогда максимальное число интенсивных параметров, или число степеней свобод, равно
| n = (k+1)r - (k+2)(r-1) = k + 2 - r |
Сопоставляя уравнения (2.35), (2.37) и (2.38), можно определить общие пределы изменения числа экстенсивных и интенсивных параметров в равновесной системе:
k + 2 ≥ ƒex = r,
0 ≤ ƒin ≤ k + 2 - r. |
(2.39) |
Соотношения (2.39) показывают что число экстенсивных параметров не может быть меньше числа фаз и максимальное число интенсивных параметров должно быть совместимо с этим. Другим крайним случаем является случай, когда система не имеет независимых интенсивных параметров (ƒin =0), а полностью задана k+2 экстенсивными параметрами. В физико-химическом анализе число независимых интенсивных параметров, характеризующее данное состояние системы, принято называть вариантностью системы, обозначая соответственно нонвариантное (n= ƒin =0), моновариантное (n= ƒin =1), дивариантное (n= ƒin =2) и т. д. состояния систем.
Термодинамические потенциалы и определение систем с вполне подвижными компонентами
В предыдущем разделе были рассмотрены четыре главных типа термодинамических систем, которые различаются факторами состояния, регулирующими тепловые и механические процессы в системах. Термодинамические потенциалы систем были получены из уравнения внутренней энергии путем приложения преобразования Лежандра, заменяющего экстенсивный параметр на сопряженный интенсивный в членах, характеризующих тепловые и механические процессы.
Распространим теперь преобразование Лежандра на члены, характеризующие химические процессы в системе. Пусть для компонентов от a до i факторами состояния остаются массы компонентов, т. е. ma,..., mi, а для компонентов от j до k факторами состояния станут сопряженные интенсивные параметры - химические потенциалы этих компонентов μj,...,μk. Тогда для того, чтобы получить выражение термодинамического потенциала такой системы необходимо вычесть из термодинамических потенциалов рассмотренных выше систем сумму произведений вида  . Это следует сделать потому, что значения факторов состояния μj,...,μk заданы одинаковыми для всей системы (изопотенциальные системы) условиями их существования и в этих системах не может совершаться полезная работа за счет выравнивания μj,...,μk по фазам, уменьшающей ее термодинамический потенциал. (Нетрудно видеть полную адекватность рассуждений, использованных ранее при выводе термодинамических потенциалов F,H и G). . Это следует сделать потому, что значения факторов состояния μj,...,μk заданы одинаковыми для всей системы (изопотенциальные системы) условиями их существования и в этих системах не может совершаться полезная работа за счет выравнивания μj,...,μk по фазам, уменьшающей ее термодинамический потенциал. (Нетрудно видеть полную адекватность рассуждений, использованных ранее при выводе термодинамических потенциалов F,H и G).
Тогда обозначив термодинамический потенциал системы с химическими потенциалами как факторами состояния через Фm, имеем общие соотношения:
 |
(2.40) |
 |
(2.41) |
Конкретизируем эти соотношения на примере реальных систем, подставляя выведенные выше выражения термодинамических потенциалов (2.26, 2.27, 2.29, 2.31) и их дифференциалов (2.25, 2.28, 2.30, 2.32). Так, для системы с набором параметров Um= ƒ(S,V, ma,..., mi, μj,...,μk) имеем
или, короче,
 |
(2.42) |
и в дифференциальной форме
 |
(2.43) |
Аналогичным образом можно получить термодинамические потенциалы систем с таким же набором факторов состояния, регулирующих химические процессы, но уже различающихся тепловым и механическим режимом: Fm = ƒ(T, V, ma,..., mi, μj,...,μk), Hm = f(S, p, ma,..., mi, μj,...,μk) и Gm = f(T, p, ma,..., mi, μj,...,μk). Приведем соответствующие выражения.
Термодинамический потенциал системы Fm = ƒ(T, V, ma,..., mi, μj,...,μk), получим в виде
 |
(2.44) |
 , , |
 |
(2.45) |
Термодинамический потенциал системы Hm = ƒ(S, p, ma,..., mi, μj,...,μk) получим в виде
 |
(2.46) |
 , , |
 |
(2.47) |
Наконец, термодинамический потенциал системы Gm = ƒ(T, p, ma,..., mi, μj,...,μk) выразится как
 , , |
 |
(2.48) |
 , , |
и
 . . |
(2.49) |
Обратимся теперь еще раз к физическому содержанию проведенного преобразования. Функции Um, Fm, Нm, Gm отличаются от рассмотренных выше термодинамических потенциалов U, F, Н и G только тем, что для части компонентов вместо массы в качестве независимых выступают интенсивные параметры - их химические потенциалы, которые поддерживаются на одинаковом для всей системы уровне, определенном условиями существования системы. Следовательно, в таких системах не может происходить уменьшение термодинамического потенциала за счет химической работы выравнивания μ по фазам этих компонентов внутри системы и соответствующие функции преобразованы совершенно аналогично тому, как это было сделано выше при переходе от внутренней энергии к другим термодинамическим потенциалам. Полученные функции Um, Fm, Нm, Gm также представляют термодинамические потенциалы. Это видно из полной симметричности преобразования, но может быть строго доказано независимо (Коржинский, 1957). Можно убедиться в том, что все они - характеристические функции, полные дифференциалы, убыль их отражает максимальную работу соответствующих систем.
Условия равновесия рассматриваемых систем:
Um = ƒ(S, V, ma,..., mi, μj,...,μk) = min, dUm = 0, d2Um > 0,
Fm = ƒ(T, V, ma,..., mi, μj,...,μk) = min, dFm = 0, d2Fm > 0,
Hm = ƒ(S, p, ma,..., mi, μj,...,μk) = min, dHm = 0, d2Hm > 0,
Gm = ƒ(T, p, ma,..., mi, μj,...,μk) = min, dGm = 0, d2Gm > 0.
|
(2.50) |
Для гетерогенных систем необходимым условием выполнения минимума термодинамического потенциала (2.50) является (как показано выше) равенство по фазам интенсивных параметров сопряженных с экстенсивными факторами состояния, т.е. для химической работы равенство химических потенциалов тех компонентов, факторами состояния которых являются массы (ma,..., mi)
Все рассматриваемые термодинамические потенциалы представляют функции k+2 независимых параметров, причем важно, что в число k для одних компонентов входят в качестве факторов состояния экстенсивные параметры - их массы, для других компонентов факторами состояния являются интенсивные параметры - их химические потенциалы.
Различающиеся термодинамическим режимом компоненты получили различное наименование. Инертными компонентами (и.к.) названы компоненты, для которых факторами состояния являются экстенсивные параметры, т. е. их массы или содержания в системе. Вполне подвижными компонентами (в. п. к.) названы компоненты, для которых факторами состояния являются интенсивные параметры, т. е. их химические потенциалы (или другие интенсивные параметры).
Наконец, в отличие от рассмотренных выше получили особое обозначение и системы: системы, в число факторов состояния которых входят химические потенциалы (или другие интенсивные параметры) ряда компонентов, названы системами с вполне подвижными компонентами (системы в. п. к.).
Термодинамическое полноправие систем с вполне подвижными компонентами не вызывает сомнения 4. Существенно, встречаются ли они и как широко в природных условиях и производственной практике? Обратимся в этой связи к принципу дифференциальной подвижности компонентов. Рассмотрев выше (глава 1, 3) несколько реакций минералообразования, мы показали, что в них, как и в любых других природных процессах, обнаруживаются две группы компонентов, характеризующиеся принципиально различным режимом. Поведение одних компонентов обусловлено их содержанием в системе, режим других связан с внешней по отношению к системе средой - в рассмотренных примерах с составом воздействующего раствора.
Нетрудно убедиться, что если этот различный режим выразить в термодинамических терминах, то принцип дифференциальной подвижности устанавливает существование в природных процессах инертных и вполне подвижных компонентов. Те компоненты, поведение которых зависит от их содержания в системе, относятся к инертным компонентам, и особенности их режима определяются тем, что независимым параметром являлась их масса. Другие компоненты, связанные с внешней средой, относятся к вполне подвижным компонентам; их режим определяется величинами химических потенциалов, которые не зависят от процессов внутри системы и обусловлены внешними условиями существования системы.
Принцип дифференциальной подвижности компонентов может быть сформулирован теперь в полном объеме: в любом геохимическом процессе компоненты, в нем участвующие, ведут себя качественно различным образом:
для одних компонентов устанавливается инертное поведение, т. е. независимыми параметрами для них являются экстенсивные параметры: массы компонентов или их содержания в системе;
для других компонентов устанавливается вполне подвижное поведение, т. е. независимыми параметрами для них являются интенсивные параметры: химические потенциалы компонентов или другие интенсивные параметры (активности, фугитивности и т. д.).
Выше, при эмпирическом обосновании принципа дифференциальной подвижности, мы прибегали к наглядному противопоставлению различной миграционной способности компонентов: вполне подвижные компоненты легко мигрируют в природных процессах, инертные, напротив, - плохо. Хотя вообще миграционная способность как-то сопоставима с режимом компонентов, тем не менее, после того как принцип дифференциальной подвижности сформулирован строго, следует отказаться от первоначальных аналогий. Принцип дифференциальной подвижности выражает термодинамические особенности формирования природных систем. При термодинамическом подходе безразлична история формирования систем - были привнесены некоторые компоненты в систему или ранее находились в ней, - важен режим компонентов в данном процессе, важно - определяется их поведение экстенсивными или интенсивными параметрами. Поэтому встречающееся отождествление миграционной способности и термодинамической подвижности компонентов, строго говоря, конечно, неправильно.
Принцип дифференциальной подвижности отражает самые общие закономерности природных процессов и является одним из главных и общих геохимических законов. Он устанавливает, что природные процессы протекают в условиях особого типа термодинамических систем - систем с вполне подвижными компонентами. Системы с вполне подвижными компонентами представляют, таким образом, термодинамическую модель природных равновесных систем и в этом их первостепенное значение. Открытие принципа дифференциальной подвижности компонентов и разработка термодинамики систем с вполне подвижными компонентами - выдающийся вклад Д. С. Коржинского в развитие естествознания. Любопытно в связи с этим заметить, что попытки распространить преобразование Лежандра на другие параметры, кроме тепловых и механических, встречаются в специальных термодинамических работах (например, П. Умовым была предложена функция вида dФ = -SdT + Vdp + Xdχ - χdX).
Однако лишенные ясного физического смысла, эти попытки не получили отклика, оставаясь формальными математическими упражнениями. Термодинамика систем с вполне подвижными компонентами - новый раздел термодинамики, разработанный Д. С. Коржинским, и становление его как всякого нового проходило не просто, отзвуками чего были жаркие дискуссии (см. Коржинский, 1957, 1972, где приведены материалы и библиография дискуссий). В настоящее время термодинамика систем с вполне подвижными компонентами успешно разрабатывается как фундаментальный раздел физической химии и физической геохимии.
Правило фаз в системах с вполне подвижными компонентами
Рассмотрим теперь правило фаз применительно к системам с вполне подвижными компонентами. Общее число независимых параметров системы ƒin + ƒex = k + 2 для систем с вполне подвижными компонентами может быть очевидным образом раскрыто как
| ƒin + ƒex = ki + km + 2 |
(2.51) |
где ki, km - соответственно число инертных и вполне подвижных компонентов. Полагая, как и выше, ƒex = r и обозначая n = ƒin, получим
| n = ki + km + 2 - r |
(2.52) |
Введем представление о внутренних степенях свободы. Под внутренними степенями свободы будем понимать те независимые интенсивные параметры, которые может иметь система при произвольных, но определенных значениях интенсивных факторов состояния. Разъясним это определение.
Термин <произвольные, но определенные> (далее в зависимости от контекста сокращенно <произвольные> или <определенные>) вместо обычного <постоянные> кажется предпочтительнее, поскольку точнее отражает существо состояния системы: он означает, что интенсивные параметры произвольны, т. е. независимы от процессов, происходящих внутри системы, но в то же время они определенны в том смысле, что их изменения должны быть совместимы с данным фазовым составом системы, т. е. не должны вызывать исчезновения или появления новых фаз системы. В зависимости от особенностей фазового состава системы, точности его определения, от целей и задач исследования диапазон возможного изменения произвольных, но определенных интенсивных факторов состояния будет различным. Чем точнее задан фазовый состав системы, тем уже интервал <определения> факторов состояния, но во всех случаях они представляют внешние параметры, независимые от внутреннего состояния системы. Например, для изотермо-изобарической системы с вполне подвижными компонентами произвольное, но определенное значение будут иметь km+2 интенсивных фактора равновесия: химические потенциалы вполне подвижных компонентов (числом km), температура и давление.
Число внутренних степеней свобод nw определяется следующим образом. Из уравнения (2.52), раскрывая число степеней свобод как сумму внешних интенсивных факторов состояния и внутренних степеней свобод n = ƒin + nw, получим
| nw = n - ƒin = ki + km + 2 - r - ƒin |
(2.53) |
Уравнение (2.53) показывает, что nw зависит от интенсивных факторов состояния, число которых в системах с вполне подвижными компонентами изменяется в пределах km ≤ ƒin ≤ km+2. Нетрудно убедиться также, что максимальное число фаз в системах с вполне подвижными компонентами при произвольных ƒin образуется в нонвариантных состояниях, когда nw = 0 и равно соответственно
| rmax = ki + km + 2 - ƒin |
(2.54) |
Общие уравнения (2.53) и (2.54) легко приводятся к формам правила фаз, соответствующим конкретным типам природных систем. Термодинамический анализ различных процессов показал, что в природных условиях осуществляются три главных типа систем с вполне подвижными компонентами: 1) изотермо-изобарические системы с вполне подвижными компонентами Gm = ƒ(T, p, ma,..., mi, μj,...,μk), которые характеризуют метаморфические и некоторые метасоматические процессы; 2) изохоро-изотермические системы с вполне подвижными компонентами Fm = ƒ(T, V, ma,..., mi, μj,...,μk), типичные для метасоматических образований, и 3) изобарно-изоэнтропические системы с вполне подвижными компонентами Hm = ƒ(S, p, ma,..., mi, μj,...,μk), которые осуществляются при эвтектической кристаллизации магматических расплавов. Для каждого типа систем можно написать соответствующую форму правила фаз (где индексы при n и r обозначают произвольные интенсивные факторы состояния):
| nT, p, μ = ki + km + 2 - r -ƒin = ki - r, rT, p, μmax = ki |
(2.55) |
| nT, μ = ki + km + 2 - r -ƒin = ki + 1 - r, rT, μmax = ki + 1 |
(2.56) |
| np, μ = ki + km + 2 - r -ƒin = ki + 1 - r, rp, μmax = ki + 1 |
(2.57) |
Полученные соотношения приводят к следующим важнейшим выводам.
1. Число фаз в системах с вполне подвижными компонентами не зависит от числа вполне подвижных компонентов и определяется экстенсивными параметрами систем, в число которых входят массы инертных компонентов, а также (в соответствующих системах) объем и энтропия.
2. Химические потенциалы вполне подвижных компонентов, являясь интенсивными факторами состояния, играют такую же роль, как температура и давление, определяя разнообразие фазового (минерального) состава и фазовых равновесий (парагенезисов), и условия их существования в системах с вполне подвижными компонентами.
Рассмотренные положения имеют фундаментальное значение для физико-химического анализа природных систем. Они показывают принципиальную особенность природных систем, состоящую в том, что число минералов в природных системах всегда меньше числа слагающих их компонентов и, напротив, разнообразие минерального состава и парагенезисов значительно шире, поскольку оно зависит не только от температуры и давления, но и от величин химических потенциалов (или других интенсивных параметров) вполне подвижных компонентов.
В свете изложенного становятся ясными неудачи первоначального применения правила фаз к анализу парагенезисов: минералогическое правило фаз Гольдшмидта (r=k) не учитывало главной особенности природных систем - вполне подвижного поведения ряда компонентов, не влияющего на число фаз. Только открытие систем с вполне подвижными компонентами и, как следствие, новая форма правила фаз создали необходимую теоретическую основу физико-химического анализа парагенезисов. Соотношения (2.55) - (2.57), впервые выведенные Д. С. Коржинским, со временем получили наименование <правила фаз Коржинского>.
Термодинамические потенциалы систем с ионизированными вполне подвижными компонентами
Многие природные процессы минералообразования протекают в присутствии водных растворов и поэтому компоненты, в них участвующие, оказываются в той или иной степени ионизированными. Нередки также в природных условиях окислительно-восстановительные процессы, которые совершаются одновременно с изменением кислотности растворов или независимо от нее.
При рассмотрении равновесий с ионизированными компонентами существенным является вопрос о правильном выборе независимых компонентов, поскольку в системах происходит взаимодействие компонентов с раствором с образованием за счет растворителя одинаковых частиц (группы Н+ и ОН-) и на системы в общем случае наложено условие электронейтральности.
В тех случаях, когда в растворе кроме Н2О присутствует какой-либо один компонент (например, Na2O), общее содержание или концентрация компонента и концентрация его ионных форм связаны константами диссоциации. Например,
| Na2O + Н2О = 2NaOH = 2Na+ + 2OH- |
и константа реакции
Учитывая Н2О = Н+ + ОН-, эту реакцию можно записать и так: Na2O + 2Н+ = 2Na+ + Н2О с константой  . В приведенных выражениях в квадратных скобках обозначены концентрации или в общем случае активности соответствующих компонентов. Поскольку К' и К" различаются величиной константы диссоциации воды и эта величина постоянная при данных T и p, то в качестве независимой равноценно может быть принята любая из форм нахождения компонента. . В приведенных выражениях в квадратных скобках обозначены концентрации или в общем случае активности соответствующих компонентов. Поскольку К' и К" различаются величиной константы диссоциации воды и эта величина постоянная при данных T и p, то в качестве независимой равноценно может быть принята любая из форм нахождения компонента.
Сложнее обстоит дело с многокомпонентными растворами. В этом случае растворение каждого из компонентов будет влиять на концентрацию ионов водорода и гидроксила, а изменение кислотности раствора, в свою очередь, будет вызывать (в соответствии с константами диссоциации) изменение концентрации ионных форм. Таким образом, общий эффект взаимодействия компонентов в растворе выразится в каком-то определенном суммарном уровне кислотности раствора и определенной общей или валовой концентрации компонента, тогда как концентрация каждой конкретной ионизированной формы будет, очевидно, находиться в зависимости от валовой концентрации компонента и кислотности раствора. Соответственно в качестве независимых параметров многокомпонентного раствора выступают суммарные валовые активности (концентрации) или химические потенциалы компонентов и активность, или, точнее, химический потенциал ионов водорода. Заметим при этом, что выбор химического потенциала иона водорода в качестве независимой переменной представляет не только рациональный термодинамический прием, но отражает условия существования природных систем, режим кислотности в которых поддерживается главным образом индифферентными (т. е. не участвующими в процессах минералообразования) вполне подвижными компонентами.
Вместе с тем следует указать, что при анализе парагенезисов часто вызывает интерес зависимость минеральных равновесий от величины химического потенциала конкретного иона, участвующего в реакции (особенно когда физико-химические данные позволяют это рассчитать). Такая зависимость с успехом может быть исследована, однако следует помнить, что активность иона зависит от кислотности раствора или - альтернативная позиция, - если химический потенциал иона принять независимым, от кислотности раствора будут зависеть общая концентрация и химический потенциал компонента (что, конечно, искусственно).
Для обобщенной характеристики процессов окисления-восстановления в качестве параметров сходным образом целесообразно принять не характеристики каких-либо конкретных окисленных или восстановленных форм компонентов, а изменение общего содержания электронов и окислительно-восстановительного потенциала (химического потенциала электрона) системы. Обратим внимание, что, затрагивая процессы окисления-восстановления, мы переходим к более сложным, нежели простые, термодинамическим системам. В этих системах происходят электрические или электрохимические процессы, которые также могут быть полностью охарактеризованы парой сопряженных параметров: экстенсивным, который отражает количество электричества, содержащегося в системе, и который в обобщенном виде можно обозначить как массу электронов me-, и интенсивным параметром, который характеризует электрическую напряженность системы и который мы аналогично тому, как это сделано для химической напряженности, обозначим как химический потенциал электрона μe-. Соответственно элементарная электрохимическая работа выразится как δZe- = μe-δme. Приведенные обозначения отличаются от общепринятых в химической термодинамике, однако они имеют преимущество своей обобщенностью и симметричностью. Нетрудно показать, и это будет сделано в дальнейшем, что масса электронов может быть привычно выражена через произведение числа зарядов на единичный заряд или число Фарадея, а химический потенциал электрона представляет суть восстановительный потенциал.
Обобщенный способ выражения реакции в растворах с изменением кислотности и степени окисления известен так же, как способ Пурбо, названный так по имени исследователя, который подчеркнул, что любая химическая (или минеральная) реакция в присутствии раствора может быть выражена в виде
| аА + bВ + сС + dD +lН2О + mН+ + ne- = 0. |
(2.58) |
В общем случае, который имеет преимущественное значение для анализа парагенезисов, кислотно-основные и окислительно-восстановительные равновесия протекают таким образом, что кислотность и степень окисления не зависят от реакций внутри системы a, определяются внешними условиями существования системы и факторами состояния являются химические потенциалы протона (иона водорода), электрона и, в силу уравнения (2.58), химический потенциал воды. Такие системы можно обозначать как системы с внешне контролируемой кислотностью и степенью окисления или системы с вполне подвижными протоном и электроном. Термодинамический потенциал изотермо-изобарической системы с вполне подвижными протоном, электроном и водой имеет вид
 , , |
(2.59) |
 . . |
(2.60) |
Наконец, в общем виде, когда кроме Н2О, Н+ и e- в системе присутствуют другие вполне подвижные компоненты, термодинамический потенциал - свободная энергия Гиббса такой системы равен:
 , , |
(2.61) |
 . . |
(2.62) |
Очевидно, что функции Umhe, Hmhe, Fmhe будут иметь подобный вид, отличаясь от Um, Hm и Fm, так же как Gmhe от Gm, выделенными членами:  и представляют, по существу, разновидности термодинамических потенциалов систем с вполне подвижными компонентами. Поэтому нет надобности повторять их характеристики, они обладают всеми свойствами термодинамических потенциалов. Далее, в соответствующих разделах мы покажем как элементарными условиями стандартизации (кстати необходимым и для всех μВ.П.К.) выражение μH+ и μe- приводится к привычным pH и Eh. и представляют, по существу, разновидности термодинамических потенциалов систем с вполне подвижными компонентами. Поэтому нет надобности повторять их характеристики, они обладают всеми свойствами термодинамических потенциалов. Далее, в соответствующих разделах мы покажем как элементарными условиями стандартизации (кстати необходимым и для всех μВ.П.К.) выражение μH+ и μe- приводится к привычным pH и Eh.
В заключение раздела уместно снова вспомнить о методе теоретического моделирования, поскольку открытие систем с вполне подвижными компонентами как термодинамической модели природных систем - блестящий пример применения метода теоретического моделирования в физической геохимии. Установление эмпирического принципа дифференциальной подвижности компонентов - этап выявления исходных посылок. На основании принципов и общих законов термодинамики выведены уравнения термодинамических потенциалов нового типа систем с вполне подвижными компонентами, представляющие теоретическую модель природных термодинамических систем. Исследование модели привело к установлению новой формы правила фаз, отражающей особенности формирования природных парагенезисов. Успешное приложение правила фаз к анализу парагенезисов (этап проверки модели), не только утвердило системы с вполне подвижными компонентами как термодинамическую модель природных систем, но и открыло широкую дорогу физико-химическому анализу парагенезисов минералов. Перейдем теперь к рассмотрению некоторых других важнейших выводов из уравнений термодинамических потенциалов, а также существенных для нашей цели термодинамических соотношений.
Термодинамические потенциалы как характеристические функции системы
Напомним, что термодинамические потенциалы служат характеристическими функциями системы в том смысле, что производная от термодинамического потенциала по термодинамическому параметру также является термодинамическим параметром. Термодинамический потенциал представляет полный дифференциал как функция k+2 независимых параметров - факторов состояния системы. В системе с k+2 независимыми параметрами все другие параметры могут быть выражены как функции этих k+2 факторов состояния.
Отмеченные свойства широко используются в термодинамике для выведения интересующих зависимостей в любых типах термодинамических систем. Рассмотрим несколько соотношений, которые будут полезны нам в дальнейшем.
Энтальпия системы с вполне подвижным компонентом является полным дифференциалом системы H = ƒ(S, p, ma,..., mi, μj,...,μk):

в тоже время
откуда очевидна зависимость энтальпии от k+2 факторов состояния системы:

Увеличение энтропии, давления и масс компонентов приводит к росту энтальпии системы пропорционально температуре, объему и химическим потенциалам компонентов, а повышение химических потенциалов уменьшает энтальпию системы пропорционально массам вполне подвижных компонентов, впрочем эти зависимости и так видны из уравнения (2.47).
Значительно более интересные соотношения могут быть получены из уравнения (2.47) как полного дифференциала путем перекрестного дифференцирования. Например:

Нетрудно убедиться, что для системы из k компонентов таких соотношений будет  . Некоторые из них, например (2.65), (2.66), (2.67), имеют ясный физический смысл, показывая каково взаимное влияние интенсивных параметров в зависимости от изменения сопряженных экстенсивных параметров. Например, уравнение (2.64), как влияет на температуру давление в зависимости от изменения сопряженных экстенсивных параметров - энтропии и объема. В других случаях (при производных интенсивных параметров по экстенсивным и наоборот), как например, уравнение (2.68) полученные соотношения не имеют реального значения или оно становится понятным после соответствующих преобразований. . Некоторые из них, например (2.65), (2.66), (2.67), имеют ясный физический смысл, показывая каково взаимное влияние интенсивных параметров в зависимости от изменения сопряженных экстенсивных параметров. Например, уравнение (2.64), как влияет на температуру давление в зависимости от изменения сопряженных экстенсивных параметров - энтропии и объема. В других случаях (при производных интенсивных параметров по экстенсивным и наоборот), как например, уравнение (2.68) полученные соотношения не имеют реального значения или оно становится понятным после соответствующих преобразований.
Рассмотрим в качестве второго примера изотермо-изобарическую систему с вполне подвижными компонентами: G = ƒ(T, p, ma,..., mi, μj,...,μk). Ее полные дифференциалы:

и
 . . |
(2.49) |
тогда

Из этих уравнений очевидны зависимости Gm-потенциала: при повышении температуры и химических потенциалов вполне подвижных компонентов он уменьшается, при увеличении объема и масс инертных компонентов - увеличивается.
Путем перекрестного дифференцирования выведем несколько полезных соотношений:

Уравнения (2.74-2.75) показывают явную зависимость химического потенциала инертного компонента а от температуры (уменьшается), давления (увеличивается) и химического потенциала вполне подвижных компонентов (уменьшается). Уравнение (2.73) не имеет столь явный физический смысл - его мы раскроем немного позже. Как уже отмечалось, в системе из k компонентов возможны  соотношения в виде частных производных, полученных перекрестным дифференцированием по факторам состояния. Эти соотношения позволяют выявить искомые взаимосвязи термодинамических параметров системы. соотношения в виде частных производных, полученных перекрестным дифференцированием по факторам состояния. Эти соотношения позволяют выявить искомые взаимосвязи термодинамических параметров системы.
Другой прием, которым можно пользоваться для установления нужных зависимостей между термодинамическими характеристиками, состоит в том, что если система задана k+2 факторами состояния, которые являются независимыми параметрами, то любой другой зависимый параметр может быть выражен в виде полного дифференциала от факторов состояния системы. Так для системы Gm = ƒ(T, p, ma,..., mi, μj,...,μk) можно выразить S = ƒ(T, p, ma,..., mi, μj,...,μk), V = ƒ(T, p, ma,..., mi, μj,...,μk), μa = ƒ(T, p, ma,..., mi, μj,...,μk), mj = ƒ(T, p, ma,..., mi, μj,...,μk) и т. д. Покажем это на примере энтропии:

Примем химическое состояние системы постоянным, т. е. dma = dmb = ... = dmi = 0, dμa = ... = dμi = 0 - тогда уравнение (2.76) предстанет в виде

Раскроем значения частных производных переходя тем самым от канонических термодинамических уравнений к обычным функциональным зависимостям. Как известно  , тогда , тогда  . Другая производная согласно (2.73) равна . Другая производная согласно (2.73) равна  , но если ввести термический коэффициент расширения α , но если ввести термический коэффициент расширения α  , то , то

Отметим, что для получения различных неканонических зависимостей между термодинамическими величинами в некоторых обстоятельных термодинамических курсах и работах используется метод якобиан (метод определителей Якоби). Он позволяет получить выражения нескольких функций от нескольких переменных. Однако заметная громоздкость вычислений и, главное, необходимость раскрывать полученные выражения через производные первичных термодинамических параметров и реальные термодинамические зависимости, делают с нашей точки зрения, предпочтительным вывод термодинамических соотношений непосредственно из уравнений термодинамических потенциалов.
Парциальные (мольные и удельные) термодинамические характеристики
Состав многокомпонентной, системы должен быть задан (описан) массами слагающих систему компонентов: ma, mb,..., mk, где масса может быть выражена или количеством весовых единиц, или количеством молей (грамм-молекул) компонента. Для физико-химического анализа систем оказывается значительно рациональней (в чем убедимся в дальнейшем), когда массы компонентов выражены в относительных единицах  , которые также могут быть весовыми или мольными долями. Тогда, если массы выражены в мольных единицах (что более употребительно), т. е. представляют мольные доли компонентов: , которые также могут быть весовыми или мольными долями. Тогда, если массы выражены в мольных единицах (что более употребительно), т. е. представляют мольные доли компонентов:
 . . |
(2.80) |
причем
 . . |
(2.81) |
Аналогичным образом в весовых единицах будем иметь:
 . . |
причем
 . . |
Обратим внимание, что мольные доли компонентов в фазах являются интенсивными параметрами, а уравнение (2.81) имеет тот же смысл, что и уравнение Гиббса-Дюгема, показывая, что по крайней мере один параметр для каждой фазы должен быть экстенсивным6.
Если разделить все экстенсивные параметры, входящие в уравнение термодинамического потенциала, на сумму масс компонентов, получим выражение удельного (если массы были в весовых единицах) или мольного термодинамического потенциала:

В дифференциальной форме соответственно:

откуда видно, что переход к мольному потенциалу осуществляется делением всех экстенсивных параметров системы на сумму масс компонентов системы, т. е. отнесением их к единичной массе системы.
Окончательно имеем

Мольные величины обычно записываются с черточкой над символам параметра  и т. д., мольный потенциал Гиббса обозначается нередко через g или ζ, соответственно в системах с в.п.к. gm, ζm, но в литературе чаще всего можно встретить запись мольного потенциала в тех же символах, что и полного и только запись количеств компонентов в виде мольных долей или масс однозначно обозначает мольный или полный потенциал. Мы будем следовать этой традиции, вводя специальные символы потенциалов только в тех случаях, когда это необходимо для правильного понимания. и т. д., мольный потенциал Гиббса обозначается нередко через g или ζ, соответственно в системах с в.п.к. gm, ζm, но в литературе чаще всего можно встретить запись мольного потенциала в тех же символах, что и полного и только запись количеств компонентов в виде мольных долей или масс однозначно обозначает мольный или полный потенциал. Мы будем следовать этой традиции, вводя специальные символы потенциалов только в тех случаях, когда это необходимо для правильного понимания.
Мольный потенциал чрезвычайно широко используется в термодинамике - как всякая "удельная" характеристика он незаменим при сравнительном анализе.
Кроме мольного потенциала в химической термодинамике широко используются удельные или мольные или, как их принято обозначать, парциальные характеристики компонентов. Парциальными (мольными или удельными) называются экстенсивные параметры, отнесенные к единице массы (количеству молей или весовых единиц) какого-либо компонента. Парциальный параметр, или парциальная величина, равен приращению соответствующего экстенсивного параметра при бесконечно малом изменении массы какого-либо компонента, происходящем при постоянстве Т, р и масс других компонентов. Согласно этому определению, если q - любой экстенсивный параметр, то

где qa, qb ... qk - парциальные величины. Для простых термодинамических систем:

- парциальные энтропия, объем, энергии и энтальпии компонента а. Так же будут выражены и парциальные характеристики всех других компонентов. Обратим внимание, что только парциальная свободная энергия Гиббса равна химическому потенциалу компонента, тогда как другие парциальные термодинамические потенциалы представляют более сложные функции:

Парциальные величины характеризуются следующими важными свойствами (приводятся без подробного доказательства, интересующиеся могут ознакомится с полным курсом химической термодинамики).
1. Первое очевидное свойство:
 . . |
(2.87) |
Разделив уравнение на , получим

2. Дифференцируя при постоянных qa,... qk, получим
 . . |
(2.89) |
 |
3. Дифференцируя (2.87) одновременно по q и m, а уравнение (2.88) по q и х и сравнивая полученные уравнения соответственно с (2.89) и (2.90), приходим к следующим зависимостям:
 , , |
(2.91) |
 . . |
(2.92) |
Обратим внимание на то, что во всех уравнениях, где массы заменены мольными долями, парциальная величина остается в соответствии с определением (2.84) частной производной по массе.
Для того чтобы нагляднее представить существо приведенных уравнений и вывести некоторые другие полезные соотношения обратимся для простоты к двухкомпонентной системе.
Прежде всего напомним, что состав бинарной системы может быть задан массами двух компонентов: mа и mb или мольной (или весовой) долей одного из них: xa или xb, т.е. в соответствии с (2.81), xa+xb=1, xb=1-xa и, дифференцируя,
 . . |
(2.93) |
Из уравнений (2.87)-(2.92) вытекают следующие важные соотношения между парциальными величинами в бинарной системе:

откуда дифференцируя по xb выведем важную формулу:

Подставляя (2.95) в (2.94) получим известное уравнение:

которое показывает изменение  в зависимости от состава бинарной системы. в зависимости от состава бинарной системы.
Уравнения (2.91) и (2.92) могут быть выражены через частные производные, давая при этом серию употребляемых в химической термодинамике соотношений (cм.подробнее Акопян, 1963, Кричевский, 1962 и др.). Например:

или, выраженные в мольных долях

и, преобразуя (2.99), получим:

или с учетом (2.93)


Рассмотренные соотношения имеют наглядное графическое изображение.
На рис. 2.3 представлена диаграмма, где по оси ординат отложена любая экстенсивная характеристика q, а по оси абсцисс - мольные доли компонентов. На диаграмме нанесена кривая q=f(x) при условии Т,р= const, на которой произвольно выбрана точка 1 и в ней проведена касательная к кривой. Ордината этой точки q1, а продолжение касательной до пересечения с осями q в точках xa = 1 (xb = 0), xb = 1 (xa = 0) и отсекает на них отрезки a1a = q1a и b1b = q1b. Это очевидно из выражения (2.67) в простейшем случае, когда qa, qb не зависят от состава, при xa = 1 получим q = q0a, а при xb = 1 соответственно q = q0b, и функция q=f(x) будет представлена прямой, соединяющей qa и qb. В общем случае, когда qa и qb изменяются в зависимости от х, принятое утверждение следует доказать. Проще всего это сделать следующим образом. Производная  в точке 1 равна dq1 / dxa = tg α1 (см. рис. 2.3). Но отрезок a1b2=ab=1, поскольку xa+xb =1. Тогда tg α1 = b1b2 / 1 = bb1 - bb2 = bb1 - aa1 = qb - qa и окончательно dq1 / dxb = q1b - q1a. Это справедливо для каждой точки кривой q=f(x), кроме, естественно, xb = 0. Таким образом, графически доказывается выведенное раньше уравнение (2.95): в точке 1 равна dq1 / dxa = tg α1 (см. рис. 2.3). Но отрезок a1b2=ab=1, поскольку xa+xb =1. Тогда tg α1 = b1b2 / 1 = bb1 - bb2 = bb1 - aa1 = qb - qa и окончательно dq1 / dxb = q1b - q1a. Это справедливо для каждой точки кривой q=f(x), кроме, естественно, xb = 0. Таким образом, графически доказывается выведенное раньше уравнение (2.95):

Уравнение (2.96) графически на рис. 2.3 выражается следующими соотношениями отрезков  . Решая его относительно q1a получим . Решая его относительно q1a получим  . Аналогично можно показать, что bb1=q1b. Тем самым дoказывается, что касательная к кривой q=f(x) отсекает по ординате при xa=0 и xb=0 соответственно парциальные величины qb и qa. Вспомним в связи с этим уже сделанное замечание о том, что только производная по массе от экстенсивного параметра представляет парциальную величину. Нетрудно видеть из выражения (2.95), что физический смысл производной по мольной доле уже иной. . Аналогично можно показать, что bb1=q1b. Тем самым дoказывается, что касательная к кривой q=f(x) отсекает по ординате при xa=0 и xb=0 соответственно парциальные величины qb и qa. Вспомним в связи с этим уже сделанное замечание о том, что только производная по массе от экстенсивного параметра представляет парциальную величину. Нетрудно видеть из выражения (2.95), что физический смысл производной по мольной доле уже иной.
Уравнения (2.70) и (2.71), их графическая интерпретация (см. рис. 2.1) имеют существенное значение для вычисления парциальных характеристик по мольным и обратно. Из приведенных выше уравнений (2.99-2.102) следует ряд важных свойств парциальных величин, но эти свойства достаточно очевидны, например, изменение парциальной величины одного компонента вызывает изменение ее и для другого компонента. Поэтому уместно их рассматривать непосредственно в приложении к конкретным задачам.
Парциальные величины в системах с вполне подвижными компонентами следует определить как приращение любого экстенсивного параметра при бесконечно малом изменении массы какого-либо компонента при постоянных температуре, давлении, химических потенциалах и массах всех других компонентов. Покажем, что парциальная величина представляет индивидуальную характеристику каждого компонента независимо от того являются в системе независимыми интенсивными параметрами только температура и давление или в их число входят химические потенциалы вполне подвижных компонентов.
Рассмотрим двухкомпонентную изотермо-изобарическую систему. Ее термодинамический потенциал G = ƒ(p, T, ma, mb) в интегральной форме равен
 . . |
(2.103) |
Производные от G по ma и от G по mb соответственно равны парциальным свободным энергиям или химическим потенциалам компонентов a и b:

Обратимся теперь к системе, где кроме инертных компонентов a и b присутствует вполне подвижный компонент j , фактором состояния которого является интенсивный параметр - его химический потенциал.
Термодинамический потенциал системы Gm = ƒ(p, T, ma, mb, μj) в интегральной форме равен
 . . |
(2.105) |
Взяв производную от Gm по ma и от Gm по mb, получим соответственно их парциальные свободные энергии - химические потенциалы:

которые никак не зависят от вполне подвижного компонента и идентичны рассмотренным выше (2.103). Представим, что из значения свободной энергии трехкомпонентной системы (a, b, j) удалена энергия приходящаяся на вполне подвижный компонент, и парциальные свободные энергии компонентов a и b остаются такими же, как и в ранее рассмотренной системе (ab).
Определим теперь значения других парциальных величин - энтропии и объема - в системах с вполне подвижными компонентами на примере той же системы Gm = ƒ(p, T, ma, mb, μj).
Возьмем производную по температуре от разных частей уравнения (2.105:

Используя приведенные выше соотношения (2.69) и (2.74), получим:

или
 , , |
(2.109) |
а также

или
 , , |
(2.110) |
и, наконец,
 , , |
(2.111) |
Аналогичным путем для парциальных объемов мы получим необходимые соотношения, взяв от разных частей уравнения (2.105) производные по давлению

Откуда, используя выведенные ранее уравнения (2.66), (2.70), получим соотношения:
 , , |
(2.114) |
 , , |
(2.115) |
 , , |
(2.116) |
полностью симметричные выведенным выше для энтропии.
Таким образом парциальные энтропии и парциальные объемы представляют индивидуальные характеристики компонентов во всех типах систем (в том числе и в системах с в.п.к.) и не зависят от режима других компонентов. В системах с в.п.к. общая энтропия и общий объем системы слагается как взвешенная (умноженная на массу) сумма парциальных энтропий и парциальных объемов всех компонентов - и инертных и вполне подвижных.
Существенным моментом в термодинамике систем с вполне подвижными компонентами является переход к удельным (мольным) характеристикам. Из интегральной формы Gm-потенциала как бы следует, что мольная доля компонента должна определяться по отношению к сумме масс инертных компонентов:

Но в таком случае оказывается, что в дифференциальном выражении gim-потенциала

члены  не будут представлять парциальные мольные энтропию и объем системы (которые равны не будут представлять парциальные мольные энтропию и объем системы (которые равны  [2.88]), а энтропию и объем системы, отнесенные к массе инертных компонентов, т. е. [2.88]), а энтропию и объем системы, отнесенные к массе инертных компонентов, т. е.  . Члены . Члены  в этом уравнении выражают не мольные доли вполне подвижных компонентов в системе, а их удельное количество приходящееся на сумму масс инертных компонентов. Уравнение dgim оказывается термодинамически некорректным, поэтому нужно либо правильно выразить термодинамический потенциал системы охватывающий только инертные компоненты (Жариков 1987), что имеет определенный смысл в некоторых частных приложениях, либо в общем случае отнести Gm к сумме масс всех компонентов. Тогда в этом уравнении выражают не мольные доли вполне подвижных компонентов в системе, а их удельное количество приходящееся на сумму масс инертных компонентов. Уравнение dgim оказывается термодинамически некорректным, поэтому нужно либо правильно выразить термодинамический потенциал системы охватывающий только инертные компоненты (Жариков 1987), что имеет определенный смысл в некоторых частных приложениях, либо в общем случае отнести Gm к сумме масс всех компонентов. Тогда

где  - мольные энтропия и объем системы, - мольные доли всех компонентов, причем сумма их всегда равна единице, (сумма мольных долей инертных компонентов не равна единице если в системе есть в.п.к.). Такой способ задания системы позволяет строго и единообразно, относя к единице массы, описать все разнообразие систем с различным термодинамическим режимом компонентов. Например, для изотермо-изохорической системы с в.п.к. от состояния, когда все компоненты вполне подвижны: - мольные энтропия и объем системы, - мольные доли всех компонентов, причем сумма их всегда равна единице, (сумма мольных долей инертных компонентов не равна единице если в системе есть в.п.к.). Такой способ задания системы позволяет строго и единообразно, относя к единице массы, описать все разнообразие систем с различным термодинамическим режимом компонентов. Например, для изотермо-изохорической системы с в.п.к. от состояния, когда все компоненты вполне подвижны:

 , до состояния где все компоненты инертны: , до состояния где все компоненты инертны:  , причем всегда , причем всегда  . .
Таким образом, удельные характеристики, симметричные парциальным величинам, можно получить взяв производную от экстенсивных параметров системы по другим экстенсивным параметрам кроме масс компонентов. Ясный физический смысл, например, имеют производные по объему:

где GV - объемная энергия (энергия единицы объема), SV - объемная энтропия (энтропия единицы объема), ρa...ρk - мольные плотности компонентов (их количества в единице объема). Если, наконец, разбить общий объем системы на сумму объемов V = V1 + V2 + ... + Vr (например объемов фаз), то частные производные типа
 , ,
вплоть до  обладают обычными свойствами парциальных величин: обладают обычными свойствами парциальных величин:  , а также , а также  (см. уравнения 2.87, 2.89). (см. уравнения 2.87, 2.89).
Химический потенциал
Из уравнения изотермо-изобарического потенциала (2.32)
на основании свойства полного дифференциала следует

Уравнения (2.119) показывают, что химический потенциал компонента представляет парциальную свободную энергию компонента и соответственно характеризуется всеми свойствами парциальных величин. Это наглядно видно (сравним с (2.87) и (2.88)) из интегрального выражения изотермо-изобарического потенциала:
 , , |
(2.120) |
или для мольного потенциала:

Дифференцируя уравнение (2.121) при постоянных μa...μk, получим, например,
Уравнение (2.122) представляет изменение изотермо-изобарического потенциала при постоянных Т и р, в системе без в.п.к., что очевидно из сопоставления (2.122) с (2.87).
Из выражения (2.121) видно:  при xa = 1, т. е. мольный изотермо-изобарический потенциал однокомпонентной системы равен химическому потенциалу компонента. Обратим внимание на следующие соотношения. Из уравнений термодинамических потенциалов различных систем следует при xa = 1, т. е. мольный изотермо-изобарический потенциал однокомпонентной системы равен химическому потенциалу компонента. Обратим внимание на следующие соотношения. Из уравнений термодинамических потенциалов различных систем следует

Существо этих равенств наглядно проступает в сравнении с уравнением (2.86)

и, дифференцируя,
 , , |
(2.120) |
только в изотермо-изобарических условиях химический потенциал компонента равен изменению парциальной свободной энергии - термодинамического потенциала системы. Парциальные термодинамические потенциалы других систем в изотермо-изобарических условиях должны быть "исправлены" на другие виды работ, если мы хотим выделить парциальную химическую энергию из общего парциального термодинамического потенциала системы. В то же время производные по массе от термодинамических потенциалов при постоянстве факторов состояния систем (уравнение 2.121) всегда равны химическим потенциалам компонентов.
Для бинарной системы из уравнений (2.94) - (2.100) непосредственно следуют важные зависимости:
 , , |
(2.125) |
 , , |
(2.126) |
| ∂g / ∂xb = μb - μa |
(2.127) |
которые подробнее рассмотрены в следующей главе. Здесь обратим внимание на то, что если производная от G-потенциала по массе компонента всегда химический потенциал компонента, то производная по мольной доле более сложное выражение - в бинарной системе она равна разности химических потенциалов компонентов.
Раскроем теперь значение химического потенциала компонента. На основании свойств уравнения (2.32) как полного дифференциала путем перекрестного дифференцирования получено соотношение:

Полагая все другие параметры постоянными и заменяя, согласно уравнению Менделеева-Клайперона V = RT / p, придем к выражению:
 |
(2.128) |
которое показывает зависимость химического потенциала компонента от его парциального давления.
Интегрируя уравнение (2.128), получим:
Физический смысл константы интегрирования виден из следующего: при pa = 1, μa = C т.е. константа представляет значение химического потeнциала компонента при стандартных условиях, когда парциальное давление компонента равно единице. Обозначим тогда C = μ0a(T), показав кроме того, что все операции мы проводим при постоянной температуре (индекс Т). В итоге получим
| μa = μ0a(T) + RTlnpa + RTlnxa |
(2.130) |
и, включив RTlnp в член μ0a(T) получим следующее выражение:
где μ0a - константа, которая уже зависит и от температуры, и от давления (ниже мы раскроем эти зависимости), и представляет химический потенциал чистого компонента (при xa = 1, μa = μ0a) при данной температуре и давлении. Обычно индексы T и p опускают, предоставляя читателю возможность судить о характере константы по выражению члена, зависящего от состава. Соответствующий член, кроме представленных уравнениями (2.120) и (2.131), может быть также выражен, как мы покажем ниже, и в единицах концентрации (весовой или мольной). Обратим внимание, что величина μ0a будет различна при разных способах задания или описания состава системы.
Два важных соотношения, непременно встречающихся в дальнейшем, получим дифференцированием уравнения (2.131):
| dμa = RT dlnxa |
(2.131) |
 |
Рассмотрим теперь зависимость химического потенциала какого-либо инертного компонента от температуры, давления и других параметров системы. Пусть задана равновесная изотермо-изобарическая система с вполне подвижными компонентами, в которой μa = ƒ(T, p, ma,..., mi, μj,...,μk) поскольку в состоянии равновесия любой параметр системы представляет однозначную функцию k+2 факторов состояния. Поэтому можно записать

Путем перекрестного дифференцирования членов уравнения Gm - термодинамического потенциала системы, как это было показано выше, получим:

Уравнения (2.66), (2.74) и (2.75) показывают, что химический потенциал (химическая энергия) компонента увеличивается с возрастанием давления и уменьшается с повышением температуры и возрастанием химического потенциала вполне подвижного компонента, пропорционально соответственно парциальным мольным объему и энтропии, а также массе вполне подвижного компонента.

Выражая, как принято количества компонентов через их мольные доли соответственно получим:

Принимая мольные доли и химические потенциалы других компонентов постоянными (или пренебрегая их влиянием на μa) и используя (2.133) получим выражение дифференциальной зависимости μa от температуры, давления и мольной доли компонента а:
| dμa = -SadT + Vadp + RT dlnxa |
(2.137) |
Сопоставляя уравнения (2.137), (2.131), (2.132), нетрудно видеть, что: а) выражение (2.132) справедливо только при постоянных Т и р; б) член μ0a включает значения Sa и Va при данных Т и р; в) при изменении Т и р величина μa изменяется в соответствии с (2.137), а величина μ0a - в соответствии с dμ0a = -SadT + Vadp. Учитывая двойственную зависимость химического потенциала от Т и р, с одной стороны, и от концентрации компонента, с другой, удобно принять следующие обозначения. Член μ0a обозначить как стандартный химический потенциал компонента, а концентрационный член RTlnxa обозначить как эффективный химический потенциал компонента. Очевидно, что вполне подвижный режим компонентов выражается через независимое изменение их эффективных химических потенциалов.
Выше, как и в большинстве разделов этой главы для выражения относительного содержания компонента использовалась его мольная доля. В определенных случаях (при практической работе нередко) целесообразно вместо мольной доли применять концентрацию компонента выражая ее через молярность (число молей растворенного компонента на 1000 см3 раствора) или моляльность (число молей растворенного вещества на 1000 г раствора).
Молярная концентрация компонента i равна
 |
(2.138) |
где V - объем раствора содержащего mi молей растворенного компонента i. Для разбавленных растворов с хорошим приближением V ≅ msolV0sol где V0sol - мольный объем растворителя. Тогда

илиподставляя последнее выражение в μi, получим
| μi = μ0i RTlnV0sol + RTlnCi = μ*i + RTlnCi |
(2.140) |
где μ0a и RTlnV0sol зависят только от T, p и природы растворителя и объединены в μ*i. При этом важно, что μ0a ≠ μ*a, а условие стандартизации μ*a = μa при концентрации раствора, равной единице (1 моль/литр). Уравнения (2.137) и (2.140) справедливы, естественно, для растворов свойства которых являются идеальными.
Обратим внимание на следующее. Если оказывается, что воздействием других компонентов на μi нельзя пренебречь, т. е. система является не идеальной, то это влияние учитывается не путем решения последних членов уравнения (2.133), а введением суммарных поправочных коэффициентов активности и заменой мольной доли в уравнениях (2.129), (2.131), (2.137) и концентрации в (2.140) на активность компонента. Рассмотрим это подробнее.
Идеальные и реальные растворы
Остановимся на краткой характеристике термодинамических свойств растворов. Как известно, по своим физико-химическим свойствам, отражающим особенности поведения компонентов, растворы разделяются на идеальные и неидеальные (или реальные).
Идеальные растворы характеризуются следующими термодинамическими признаками.
1. Парциальные мольные объемы компонентов не зависят от состава и концентрации раствора, объемный эффект смешения равен нулю:
1. Парциальные мольные объемы компонентов не зависят от состава и концентрации раствора, объемный эффект смешения равен нулю:
| Vi = V0i (при 0 < xi ≤ 1), ΔVmix = 0, |
(2.141) |
откуда непосредственно следует

2. Парциальные мольные энтальпии и энергии компонентов не зависят от состава и концентрации раствора, или, что то же, теплота (энтальпия) и энергия смешения равны нулю:
| Hi = H0i (при 0 < xi ≤ 1), ΔHmix = 0, |
(2.143) |
| Ui = U0i (при 0 < xi ≤ 1), ΔUmix = 0, |
(2.144) |
откуда также следует:

3. Парциальная мольная энтропия компонента при растворении возрастает на величину, равную -Rlnxi:
| ΔSimix = Si - S0i =-Rlnxi, |
(2.147) |
и для всего раствора

Из последнего заключения можно сделать вывод о том, что причина образования идеального раствора состоит в возрастании энтропии при смешении. Этот вывод не столь очевиден, как первые два свойства, покажем его кратко. Взяв производную по температуре от уравнения (2.131) для i-ого компонента, получим:
 но, согласно (2.74), но, согласно (2.74),

подставляя сразу, имеем искомое:
| ΔSimix = Si - S0i = -Rlnxi, |
(2.147) |
Согласно свойствам парциальных величин (уравнение 2.88):

тогда энтропия смешения всех компонентов раствора

4. Термодинамический потенциал раствора, как было показано выше, равен:

или, подставляя μa,

Свободная энергия смешения в соответствии с (2.144) выразится как

поскольку нередко принято выражать μa через  , то уравнение (2.145) можно записать как , то уравнение (2.145) можно записать как


Из уравнений (2.150)-(2.152) следует, что свободная энергия (термодинамический потенциал) уменьшается при образовании идеального раствора и соответственно всегда меньше, чем у механической смеси того же состава. Этот вывод очевиден и из соотношения ΔGmix = ΔHmix - TΔSmix: при ΔHmix = 0 и ΔSmix > 0 ΔGmix < 0. Для иллюстрации полученных зависимостей на рис.2.4 представлены графики V=f(x), H=f(x), S=f(x) и G=f(x) для бинарного идеального раствора.
Рассмотренные соотношения представляют фундаментальное определение идеальных растворов. Только соблюдение всех условий обеспечивает такие свойства растворов, которые определяются как идеальные. Используя эти соотношения, а также установленные ранее общие термодинамические зависимости, можно описать различные термодинамические свойства идеальных растворов.
Обратим внимание на следующее. Вместо перечисленных выше условий идеальности можно равнозначно определить идеальный раствор как таковой, для которого, в определенной области Т и p, для всех компонентов выполняется соотношение:
| μi = μi0 + RTlnxi, |
(2.131) |
т. е. химический потенциал любого компонента зависит только от Т и p и мольной доли (или концентраций, или парциального давления) этого компонента. Из уравнения (2.131) (сходно тому, как показано условие ΔSimix = - Rlnxi) выводятся все названные выше условия идеальности.
В принципе, рассмотренные условия идеальности полностью равнозначны. Первые имеют более наглядный физический смысл, вторые - более общее и компактное, поэтому использование их определяется конкретными задачами изложения или исследования.
Неидеальными растворами называют такие, для которых не выполняется по крайней мере одно из перечисленных условий идеальности. Существует несколько различных классификаций неидеальных растворов, но с термодинамических позиций доминирует разделение растворов в зависимости от нарушенных (и выполненных) трех условий идеальности. Выделяют:
а) регулярные растворы, для которых

и б) атермические растворы, в которых

Такое разделение существенно для вычисления различных термодинамических параметров растворов, но для нашей цели предпочтительно вначале обратиться к обобщенной характеристике неидеальных растворов. Такая обобщенная характеристика состоит в введении особой термодинамической функции (что было впервые сделано Г.Льюисом), называемой термодинамической активностью, или просто активностью. Активность i-ого компонента ai определяется cоотношением где xi - мольная доля компонента i, а γi коэффициент активости i-ого компонента, суммарно отражающий отклонение режима компонента от идеального. Тогда химический потециал i-го компонента будет равен
| μi = μi0 + RTlnai, |
(2.154) |
Уравнение (2.154) является фундаментальной зависимостью термодинамики неидеальных растворов. Оно показывает, что реальные растворы подчиняются всем законам идеальных растворов и на них распространяются все термодинамические соотношения, если вместо мольной доли (или соответствующего ее параметра) состав раствора будет охарактеризован термодинамической активностью компонента. Несколько упрощая, можно сказать, что активность представляет реальную термодинамическую или эффективную концентрацию неидеального раствора.
Первостепенное значение имеет установление соотношений между активностью и формами задания или описания состава растворов, а также необходимых при этом условий стандартизации.
Активность связана с мольной долей или концентрацией компонента следующей зависимостью: илигде γi - коэффициент активности, выражающий степень отклонения раствора от идеального поведения. Состояния, когда γi > 1, называют положительными отклонениями от идеальности, состояния γi < 1 - отрицательными, тогда как γi = 1 очевидно характеризует идеальный раствор. Коэффициент активности зависит от индивидуальных свойств вещества, от температуры, давления, состава, концентрации растворов и имеет различное значение при разных способах выражения концентрации раствора (γi ≠ γi*, так как xi ≠ Ci). В качестве стандартных состояний для твердых и жидких растворов принимают состояние чистого компонента, полагая, что в этом состоянии γi = 1 и ai=1. Однако для жидких растворов существует и другой выбор стандартного состояния, когда для растворителя принимают а=1 при x=1, а для растворенного компонента i в качестве стандартного выбирают бесконечно разбавленный раствор, полагая ai → xi при xi → 0 и приблизительно lim γi = 1 при xi → 0. Такая стандартизация имеет ясный физический смысл: при уменьшении концентрации растворы все более приближаются к идеальным.
Выражение химического потенциала через молярную концентрацию справедливо, как мы отмечали, для идеальных растворов и если при C=1 моль/литр μ0 ≠ μi0, то γi* также отлично от нуля и ai → Ci при γi* → 1 по мере разбавления раствора.
Для газовых смесей введение активностей оказывается недостаточно для полного описания отклонений газов от идеального режима. Установлено, что поведение многих индивидуальных однокомпонентных газов при различных Т и р отличается от идеального. Для термодинамической характеристики таких газов введено понятие фугитивности или летучести (предложенное также Г. Льюисом), которое определяется соотношением

где ƒ - летучесть,  - значение изотермо-изобарического потенциала, зависящее только от температуры. Для однокомпонентной системы - значение изотермо-изобарического потенциала, зависящее только от температуры. Для однокомпонентной системы  = μ, тогда, сравнивая с (2.126), уравнение (2.135) можно представить как = μ, тогда, сравнивая с (2.126), уравнение (2.135) можно представить как
| μi = μ0i(T) + RTlnƒi0, |
(2.157) |
где ƒi0 - летучесть чистого газового компонента, поскольку символом ƒi обозначается обычно летучесть компонента i в газовой смеси в соответствии с зависимостьюФизическую сущность летучести можно наглядно представить, взяв производную по р от (2.157) при T = const:

Подставляя значение левой части (из уравнения (2.66)), преобразовывая и переходя к обычной производной, получим
 |
(2.138) |
Нетрудно убедиться, что если газ характеризуется идеальными свойствами, т. е. подчиняется закону pV=RT, то dlnƒi0 = dlnpi. Если это соотношение нарушается, то летучесть представляет эффективное газовое давление, которое определяется зависимостью Vi от давления или в общем виде сжимаемостью газа:
 , , |
(2.160) |
где z = 1 для идеального газа, z > l характеризует положительные, а z < 1 отрицательные отклонения от идеальности. Отклонение газов от идеальности может быть в общем виде оценено через коэффициент летучести или фугитивности φi, определяемый соотношением
Коэффициент летучести зависит от Т, р, индивидуальных свойств газов и может быть с известным приближением рассчитан. В качестве стандартного состояния при расчетах летучестей принимается условие, когда давление равно одной атмосфере (т. е. φi = 1 при p=1 атм).
Кроме отклонений индивидуальных газов от идеальности в зависимости от Т и р следует, так же как для жидких и твердых растворов, через активности охарактеризовать поведение газов в смесях. Из известных зависимостей (легко вспомнить законы Рауля): нетрудно видеть, что отношения ƒi/ƒ0i и pi/pi0 равны мольной доле идеального и реального газа в идеальной газовой смеси (растворе). Для неидеальной газовой смеси по аналогии с жидкими растворами это соотношение должно быть исправлено на коэффициент активности. Тогда
 , , |
(2.163) |
и
 , , |
(2.163) |
где аi - активность газового компонента. Химический потенциал газового компонента в неидеальной смеси имеет такое же выражение, как и для жидкого раствора:
| μi = μ0i + RTlnai = μ0i + RTlnxi + RTlnγi, |
(2.165) |
Условия стандартизации газовых растворов аналогичны жидким: при определенных Т и р ai → 1 при xi → 1 и при xi → 1 γi → 1.
Поскольку в реальных растворах химический потенциал компонента зависит от активности компонента, уравнения мольного термодинамического потенциала и химического потенциала в дифференциальной форме будут иметь вид
| dμi = -SidT + Vidp + RTdlnai = -SidT + Vidp + RTdlnxi + RTdlnγi, |
(2.166) |
Сопоставляя это выражение с уравнениями (2.133) и (2.134) можно видеть, что член RTdlnγi выражает влияние других компонентов на μi, описывая отклонение от идеальности компонента i.
Рассмотрим теперь некоторые главные термодинамические функции реальных растворов.
Мольный изотермо-изобарический потенциал реального раствора будет равен

Сопоставляя это выражение с уравнением (2.150), нетрудно видеть, что первые два члена уравнения (2.167) равны уравнению (2.150) и представляют термодинамический потенциал идеального раствора. Тогда уравнение (2.167) можно представить как

т. е. свободная энергия реального раствора равна сумме свободной энергии идеального раствора (2.150)

и некоторой величине свободной энергии, возникающей в растворе за счет отклонения от идеальности. Последнюю функцию обозначают термином "избыточная свободная энергия", она равна:

Свободная энергия смешения неидеального раствора определится соотношением

или

Симметричным образом для характеристики отклонения растворов от идеальности введены другие избыточные термодинамические функции.
Энтропия раствора

где SI - энтропия идеального раствора; SE - избыточная энтропия. Энтальпия раствора

Объем раствора

где  - избыточные энтальпии и объем, а - избыточные энтальпии и объем, а  - соответствующие функции смешения неидеальных растворов. - соответствующие функции смешения неидеальных растворов.
Наконец, для полной симметрии обозначим как избыточный химический потенциал член RTlnγi в выражении (2.162) химического потенциала неидеального раствора, т. е. и
| μi = μiE + μiI = μi0 + RTlnγi + RTlnxi, |
(2.176) |

Для более наглядной характеристики избыточных термодинамических функций, их связи с активностями компонентов на рис. 2.5 представлены некоторые типичные соотношения для бинарного раствора, который характеризуется положительными отклонениями от идеальности с соотношениями HE > TSE > GE и приблизительно симметричными графиками этих функций. Отметим, что отклонения могут быть и отрицательными, и знакопеременными для всех избыточных функций. Однако при этом кривая зависимости G = GE + GI от активности компонентов всегда будет вогнутой (вниз), а кривая зависимости S = SE + SI выпуклой (вверх), так как в противном случае раствор будет распадаться на механическую cмесь в области составов, где термодинамический потенциал раствора окажется больше, а энтропия меньше, чем у механической смеси
Уравнение смещенного равновесия и вытекающие из него законы
Рассмотрим изотермо-изобарическую систему с вполне подвижными компонентами. Обозначим через I и II два каких-либо состояния системы. Эти состояния будут находиться в равновесии, если GIm = GIIm, так как в противном случае система самопроизвольно переходила бы в состояние с меньшей свободной энергией. Если мы будем изменять факторы состояния, то равновесие сохранится, если dGIm = dGIIm, или, раскрывая значения свободной энергии:
 . . |
Сгруппируем члены:
 . . |
В этом выражении член  равны нулю, так как в условиях равновесия химические потенциалы компонентов для различных частей или состояния системы равны, а поэтому равны нулю, так как в условиях равновесия химические потенциалы компонентов для различных частей или состояния системы равны, а поэтому  . В результате имеем . В результате имеем
 , , |
(2.177) |
где  , ,  , ,  и так до и так до  изменение энтропии, объема и масс компонентов при переходе из одного равновесного состояния в другое. Уравнение (2.177) носит название уравнения (пpинципa) смещенного равновесия: оно показывает связь между изменениями интенсивных и экстенсивных параметров, существующую в равновесной системе при изменении факторов состояния. Уравнение смещенного равновесия представляет фундаментальную характеристику фазовых соотношений. Из уравнения как частные следствия вытекают многие важные термодинамические законы и уравнения, такие, например, как уравнение Клаузиуса-Клапейрона, закон действующих масс и т. д. Рассмотрим некоторые следствия. изменение энтропии, объема и масс компонентов при переходе из одного равновесного состояния в другое. Уравнение (2.177) носит название уравнения (пpинципa) смещенного равновесия: оно показывает связь между изменениями интенсивных и экстенсивных параметров, существующую в равновесной системе при изменении факторов состояния. Уравнение смещенного равновесия представляет фундаментальную характеристику фазовых соотношений. Из уравнения как частные следствия вытекают многие важные термодинамические законы и уравнения, такие, например, как уравнение Клаузиуса-Клапейрона, закон действующих масс и т. д. Рассмотрим некоторые следствия.
Ограничимся условиями постоянства химических потенциалов вполне подвижных компонентов, т. е. dμj = ... = dμk = 0, тогда уравнение (2.177) сведется к следующему:
 , , |
откуда
 , , |
(2.178) |
Уравнение (2.178) носит название уравнения Клаузиуса-Клапейрона. Оно показывает взаимосвязь между тепловым ( или или  ) и объемным ( ) и объемным ( ) эффектами реакции перехода системы из одного состояния в другое и значениями соответствующих интенсивных параметров системы - температуры и давления. ) эффектами реакции перехода системы из одного состояния в другое и значениями соответствующих интенсивных параметров системы - температуры и давления.
Для однокомпонентной системы это разница между энтропиями и объемами двух фаз (например А и В) для моновариантной реакции A=B, т. е.  , которая изобразится моновариантной линией на диаграмме с координатами Т и р. В двухкомпонентной системе уравнение Клаузиуса-Клапейрона будет описывать трехфазовую моновариантную реакцию, отвечающую соответствующей моновариантной линии на Т-р диаграмме и так до систем с k компонентами, где в моновариантном (n=1) равновесии находятся r=k+1 фаз. , которая изобразится моновариантной линией на диаграмме с координатами Т и р. В двухкомпонентной системе уравнение Клаузиуса-Клапейрона будет описывать трехфазовую моновариантную реакцию, отвечающую соответствующей моновариантной линии на Т-р диаграмме и так до систем с k компонентами, где в моновариантном (n=1) равновесии находятся r=k+1 фаз.
Во всех случаях когда число компонентов больше одного в уравнении Клаузиуса-Клайперона ΔS и ΔV представляет изменение энтропии и объема всей системы и для многофазовой реакции должны быть учтены массы реагирующих фаз и баланс слагающих их компонентов. Обычно для этого используются уравнения Гиббса-Дюгема, характеризующих каждую фазу и сумма этих однородных линейных уравнений решают методом детерминант (определителей). Отсылая читателя за подробным выводом к углубленным курсам термодинамики и нижеследующим разделам книги (см. разделы главы III 4 и 6), приведем здесь итоговую формулу в общем виде7
 , , |
(2.178) |
для k компонентной системы и моновариантного равновесия r = k + 1 фаз. В уравнении (2.179) детерминанты равны

Заметим, что если мы имеем дело с фазами переменного состава, оказывается удобным матрицы  и и  составлять в мольных долях компонентов. составлять в мольных долях компонентов.
Рассмотренные соотношения имеют наглядную и широко используемую в физико-химическом анализе графическую интерпретацию. На рисунке 2.6, где по оси ординат отложена температура, а по оси абсцисс - давление, dT/dp представляет собой тангенс угла наклона касательных к моновариантным линиям, ограничивающим два каких-либо состояния системы и находящимся в равновесии на этой моновариантной линии.
Интегрируя (2.178) и (2.179) - ∫ΔSdT + ∫ΔVdp = const получим уравнения соответствующих моновариантных линий. Отметим, что интегрирование уравнение Клаузиуса-Клапейрона, представляет нелегкую задачу (в связи с зависимостью ΔS от Т и ΔV от p), которую мы рассмотрим в дальнейшем, в специальной главе.
Зададимся теперь условиями, когда температура и химические потенциалы всех вполне подвижных компонентов, кроме компонента j, постоянны, т. е. dT = 0, dμj+1 = ... = dμk = 0 тогда ΔVdp - Δmjdμj = 0, откуда
 , , |
(2.180) |
Уравнение (2.180) показывает связь между объемным эффектом реакции и изменением содержания вполне подвижного компонента, существующую в системе при равновесном переходе от одного состояния в другое при изменении интенсивных факторов состояния - давления и химического потенциала вполне подвижного компонента. На диаграмме в координатах μj - p (см. фиг.2.6) уравнение (2.180) выражает тангенс угла наклона касательной к моновариантной k+1 фазовой линии, а интеграл -∫Δmjdμj + ∫ΔVdp = const описывает уравнения моновариантных линий в координатах μj - p.
Наконец, рассмотрим условия, когда температура и давление постоянны, т. е. dT=0; dp=0. Тогда уравнение (2.177) предстанет в виде
 , , |
(2.181) |
Соотношение (2.181) является одной из форм выражения закона действующих масс, который устанавливает зависимость между изменениями масс и химических потенциалов или активностей компонентов для соответствующих равновесных состояний системы. Например, в системе, где изменяются химические потенциалы только двух компонентов, зависимость
 |
(2.182) |
также характеризует тангенс угла наклона касательной, а интеграл -∫Δmjdμj - ∫Δmkdμk = const представляет уравнение моновариантной линии на диаграмме μj-μk (см. рис. 2.6).
Придадим выражению закона действующих масс более обычную форму. Для этого нам необходимо проинтегрировать уравнение (2.181). Это можно сделать непосредственно, полагая, что массы компонентов не зависят от их химических потенциалов, и определив пределы интегрирования, но проще вспомнить, что интегральное выражение химического потенциала (уравнение (2.154)) равно μj = μj0 + RTlnaj. Тогда (2.181) при интегрировании превращается в следующее уравнение
 |
(2.183) |
Откуда путем несложных преобразований выводится соотношение
 |
(2.184) |
которое и представляет закон действующих масс в раскрытой логарифмической форме. Поскольку уравнение справедливо для любого числа реагирующих компoнентов, пределы суммирования в выражении (2.184) обычно опускаются, а компонент обозначается любой буквой, например i:
 |
(2.184) |
Потенциируя уравнение (2.184) получим в левой части произведение активностей компонентов, которое обычно обозначается как ∏aiΔmi, а в правой части - величину exp (  ) = ) =  , которая является постоянной при данных температуре и давлении и называется константой равновесия реакции. В результате получим , которая является постоянной при данных температуре и давлении и называется константой равновесия реакции. В результате получим
∏aiΔmi =  = exp ( = exp (  ) ) |
(2.185) |
обычную нелогарифмическую форму записи уравнения закона действующих масс. Обратим внимание на то, что во всех формулах (2.181) - (2.184) и ниже компоненты выражены алгебраической суммой или произведением активностей (2.185). Реальные знаки Δmj...Δmk зависят от уравнения соответствующих реакции и способа их записи (как процессов, происходящих внутри системы или вызванных внешним воздействием в.п.к.).
Закон действующих масс является главным термодинамическим соотношением, описывающим зависимость химических равновесий в системе. Рассмотрим подробнее некоторые существенные аспекты закона действующих масс.
Установим прежде всего важную термодинамическую зависимость, связывающую константу равновесия с изменением изотермо-изобарического потенциала соответствующей реакции. Как было показано выше (уравнения (2.150), (2.167) и др.), изотермо-изобарический потенциал может быть представлен в виде где  . Сравнивая два равновесных состояния системы А и В, получим:илиНо из (2.184) тогда окончательно получим . Сравнивая два равновесных состояния системы А и В, получим:илиНо из (2.184) тогда окончательно получим
 |
(2.186) |
Уравнение (2.186) показывает, что константа равновесия определяется величиной изобарно-изотермического потенциала реакции. Оно служит для расчета констант равновесия реакций.
Наконец, уравнение (2.184) можно преобразовать, выражая в явной форме избыточные функции неидеальных растворов. Сопоставляя рассмотренные термодинамические зависимости, можно вывести следующие соотношения: или
 |
(2.187) |
и, наконец,
 |
(2.188) |
где KpE - "избыточная" константа реакции, связанная с отклонением растворов от идеальности, равная KpE = exp (  ) или ln KpE = ) или ln KpE =  . Уравнение (2.188) может быть представлено и в нелогарифмической форме. . Уравнение (2.188) может быть представлено и в нелогарифмической форме.
| ∏xiΔmi = Kp0 . KpE = Kp |
(2.189) |
Выразим константу равновесия неидеального раствора через стандартную и избыточную свободную энергию. Опуская подробные выкладки, сделанные нами выше из сопоставления уравнений (2.186), (2.187) и (2.188) легко вывести следующее уравнение
| RT ln Kp = - (ΔG0 + ΔGE). |
(2.190) |
Рассмотрим еще два важных соотношения, показывающих зависимость константы равновесия реакции от температуры и давления. Проще всего это сделать следующим образом. В соответствии с рассмотренными зависимостями можно записать: и уравнение смещенного равновесия предстанет в виде:
| -ΔSdT + ΔVdp + RT dln Kp0 = 0 |
(2.191) |
Из уравнения (2.191) непосредственно следуют уравнение изобары реакции (уравнение Вант-Гоффа), показывающее зависимость константы равновесия от температуры:
 |
(2.192) |
и уравнение изотермы реакции, показывающее зависимость константы равновесия от давления:
 |
(2.193) |
Таким образом, во всех приведенных выражениях закона действующих масс фигурирует термодинамическая константа равновесия, записанная через активности и мольные доли компонентов. При расчетах нередко удобнее выразить количества компонентов в виде мольных масс (количествах молей) или в объемных концентрациях. Тогда для идеальных растворов "мольная" константа Km будет равна а концентрационная (Kc):где под знаком П, как и выше стоят алгебраические произведения мольных масс или концентраций.
Естественно, что Kp, Km, Kc имеют различное значение (если ∑Δmi не равно нулю). Соотношения между константами (которые выводятся подстановками xi = mi / ∑m и Ci = mi / V, что мы опускаем) следующие:

В случае ∑Δmi = 0, т. е. реакция не сопровождается изменением числа молей, значения констант совпадают.
Для газовых смесей закон действующих масс можно выразить через парциальные давления:

Отметим, что собственно для газовых смесей закон действующих масс был и сформулирован впервые исходя из молекулярно-кинетических соображений, и уже позднее получил полное термодинамическое истолкование.
Как уже подчеркивалось, природные процессы представляют неразрывное сочетание равновесных состояний с общим необратимым течением процессов. Естественным поэтому выглядит стремление распространить термодинамический аппарат на описание и исследование кинетики и динамики природных процессов, т. е. всех тех явлений, которые вызывают необратимые изменения природных систем. Такой общий подход оказывается возможным благодаря развитию методов термодинамики неравновесных, точнее, необратимых процессов. В этом разделе рассмотрим основные понятия и принципы термодинамики необратимых процессов, необходимые для использования в дальнейшем методов необратимой термодинамики при анализе кинетики и динамики природных процессов минералообразования.
Термодинамика необратимых процессов базируется на обобщении классической термодинамики и новых принципов, отражающих главные феноменологические законы необратимых изменений систем. Главными законами необратимой термодинамики являются: уравнения возрастания и скорости возрастания энтропии; закон линейных соотношений потоков и сил; принцип взаимности; закон линейной скорости возрастания энтропии при стационарных состояниях. Рассмотрим эти главные соотношения.
Энтропия и термодинамические принципы необратимых процессов
При выводе уравнений термодинамических потенциалов во всех уравнениях присутствовал член δQi, обозначенный как <некомпенсированное тепло> и выражающий возрастание энтропии или уменьшение термодинамического потенциала при необратимом стремлении системы к равновесию. Обозначив для необратимого процесса, целесообразно отметить обратимый теплообмен системы с окружающей средой как Заметим, что δQi всегда величина положительная, тогда как знак δQe зависит от направления потока тепла. Суммарная тепловая работа δQ = δQe - δQi, откуда видно, что δQ = δQe = max только когда δQi = 0. Обычно δQ < δQe поскольку δQi > 0. Иначе говоря теплообмен системы с окружающей средой максимален при обратимых процессах и всегда меньше при необратимых вследствие расхода части тепла на естественное необратимое возрастание энтропии.
Как было показано выше, изменение внутренней энергии
Введя дополнительные обозначения δQe, δAe, δWe для обратимых процессов и преобразуя, получим:
 |
(2.203) |
Нетрудно убедиться, что заключенная в скобки часть уравнения (2.203) представляет обобщенное выражение термодинамического потенциала системы, точнее, той его части, которая изменяется (уменьшается) в результате необратимых процессов в системе при постоянных факторах состояния. В зависимости от термодинамического типа системы, т.e. от набора факторов состояния, это выражение можно раскрыть через уравнение термодинамического потенциала соответствующей системы.
Изохоро-изоэнтропическая система U=ƒ(S,V,ma,...,mk) при постоянстве факторов состояния характеризуется отсутствием обратимого обмена с окружающей средой теплом, механической и химической работой. Для такой изохоро-изоэнтропической системы δQe=0, δAe=0, δWe=0 и, обозначив через diU изменение внутренней энергии, вследствие необратимых процессов из (2.203) получим
 |
(2.203) |
Это уравнение выражает изменение необратимой энтропии через изменение внутренней энергии, представляющей термодинамический потенциал изохоро-изоэнтропической системы. Необратимая энтропия возрастает при всех необратимых процессах, протекающих с уменьшением внутренней энергии.
Как было показано выше, уменьшение термодинамического потенциала системы при постоянных факторах состояния происходит путем изменения (выравнивания по фазам) интенсивных параметров системы, сопряженных с экстенсивными факторами состояния. В изохоро-изоэнтропической системе, где возможно неравенство по фазам или частям системы температур, давлений и химических потенциалов компонентов, уменьшение внутренней энергии происходит за счет потоков тепла от более нагретых частей системы к менее нагретым, потоков вещества из частей с более высокими химическими потенциалами, перемещение вещества вследствие разностей в давлении. Необходимым условием потоков является существование градиентов соответствующих интенсивных параметров.
Как было показано выше, уменьшение термодинамического потенциала системы при постоянных факторах состояния происходит путем изменения (выравнивания по фазам) интенсивных параметров системы, сопряженных с экстенсивными факторами состояния. В изохоро-изоэнтропической системе, где возможно неравенство по фазам или частям системы температур, давлений и химических потенциалов компонентов, уменьшение внутренней энергии происходит за счет потоков тепла от более нагретых частей системы к менее нагретым, потоков вещества из частей с более высокими химическими потенциалами, перемещение вещества вследствие разностей в давлении. Необходимым условием потоков является существование градиентов соответствующих интенсивных параметров.
Иногда для одномерного (х) пространства, где градиенты ∂T/∂x, ∂p/∂x и ∂μ/∂x, возрастание энтропии, или уменьшение термодинамического потенциала, выразится уравнением:

Для многомерной непрерывной системы градиенты интенсивных параметров в общем случае многомерны и выражаются обычно через оператор Гамильтона (∇T = gradx,y,zT и т. д.).

Придадим уравнению (2.206) общий вид. Для этого: 1) заменим dS на dQ/T и соответственно первый член представим  ; 2) внесем - {{1} \over {T}} под знак оператора в других членах; 3) обозначим необратимую энтропию символом U, отмечая ее принадлежность к изохоро-изоэнтропической системе. Окончательно получим: ; 2) внесем - {{1} \over {T}} под знак оператора в других членах; 3) обозначим необратимую энтропию символом U, отмечая ее принадлежность к изохоро-изоэнтропической системе. Окончательно получим:

Это уравнение носит название уравнения возрастания (или производства) энтропии и является одним из основных в необратимой термодинамике. Вывод его ясно выражает принципиальную связь равновесной и необратимой термодинамики.
Возьмем от уравнения (2.207) производную по времени, полагая, что градиенты от него не зависят, а являются функциями пространства. В результате получим уравнение скорости возрастания или скорости производства энтропии:

Выражение (2.208) представляет фундаментальное уравнение термодинамики необратимых процессов, выражающее скорость возрастания энтропии через изменение внутренней энергии и канонических параметров термодинамических систем.
Раскроем теперь через термодинамические потенциалы возрастание энтропии для других типов термодинамических систем. В изохоро-изотермической системе F=ƒ(T, V, ma,..., mk), при постоянстве факторов состояния, могут происходить процессы обратимого теплообмена с окружающей средой, т. е. δQe ≠ 0, тогда как изменение механической и химической энергии происходит вследствие необратимых процессов, т. е. δAe=0, δWe=0.
Уравнение изменения необратимой энтропии для этой системы выразится как
 |
(2.203) |
показывая, что возрастание необратимой энтропии происходит вследствие необратимого уменьшения свободной энергии (diF), представляющей термодинамический потенциал этой системы.
Уравнение (2.209) можно раскрыть различными способами. Но в основе их лежит одинаковый физический смысл, отражающий то, что в изотермической системе не могут происходить необратимые процессы переноса тепла, но могут осуществляться таковые за счет разности (градиентов) давлений и химических потенциалов. Тогда повторяя проделанные выше операции, но уже для изотермо-изохорической системы, получим для многокомпонентной непрерывной системы
 |
(2.209) |
- уравнение возрастания энтропии, а взяв производную по времени, полагая градиенты от него независимыми, получим:

По-видимому, не требует особых пояснений дальнейшее распространение симметричных преобразований на другие канонические типы термодинамических систем. Приведем соответствующие выражения через термодинамические потенциалы для уравнений возрастания и скорости возрастания энтропии.
Для системы H = ƒ(S, p, ma,..., mk):

Для системы G = ƒ(T, p, ma,..., mk):

К термодинамическим системам с вполне подвижными компонентами, как было показано выше, относятся такие системы, в число факторов состояния которых входят химические потенциалы вполне подвижных компонентов. Такие системы являются изопотенциальными, для них возможны обратимые процессы обмена с окружающей средой массами вполне подвижных компонентов. Естественно, что при постоянстве факторов состояния необратимая энтропия не может возрастать за счет химической энергии вполне подвижных компонентов и соответствующий член  должен быть изъят из уравнений, характеризующих необратимые процессы в системах. Запишем это в общем виде: должен быть изъят из уравнений, характеризующих необратимые процессы в системах. Запишем это в общем виде:

где diSФm - возрастание энтропии в системе с в.п.к., Ф - любой термодинамический потенциал обычной системы, Фm - любой термодинамический потенциал системы с в.п.к.. Скорость возрастания энтропии выразится как
 |
(2.217) |
Проведя необходимые преобразования (мы опускаем их ввиду полной идентичности с проведенными выше), получим систему уравнений возрастания и скорости возрастания энтропии, выраженную через термодинамические потенциалы для систем с вполне подвижными компонентами.

Выведенные здесь и выше уравнения возрастания (<производства>) и скорости возрастания энтропии, выраженные через уменьшение и скорости уменьшения термодинамических потенциалов, представляют характеристические уравнения необратимых процессов в простых термодинамических системах, включая системы с вполне подвижными компонентами. Эти уравнения показывают зависимость приращения и скорости приращения энтропии от изменения канонических термодинамических параметров системы.
Следует заметить, что характеристика необратимых процессов через изменение термодинамического потенциала системы имеет определенные преимущества. Они обусловлены тем, что термодинамический потенциал всегда представляет характеристическую функцию системы, тогда как описание необратимых изменений через возрастание энтропии для определенных систем в известной мере искусственно. Так, при необратимых процессах в изоэнтропических системах энтропия их (при постоянстве факторов состояния) остается, конечно, постоянной, но происходит уменьшение внутренней энергии за счет рассеяния ее во внешнюю среду, т.е. происходит увеличение diS за счет уменьшения deS.
Заметим также, что причины вызывающие необратимые процессы, или, как принято их обозначать, - действующие силы, не просто градиенты интенсивных параметров, а ∇(1/T), ∇(p/T), ∇(μ/T). Это имеет существенное значение для правильного понимания и описания неизотермических процессов, отражая определенный доминант температуры перед другими интенсивными параметрами8. Естественно, что для изотермических процессов и систем температура как постоянная величина может быть вынесена за знак градиентов. При этом необратимые изменения в системе непосредственно равны уменьшению термодинамического потенциала. Вынося T за знак градиента, вместо (2.224) и (2.225), например, получим:
 |
(2.226) |
и
 |
(2.226) |
Сопоставляя (2.224, 2.225) и (2.226, 2.227) можно видеть, что в последнем случае
 |
(2.228) |
и
 . . |
(2.229) |
Отметим, что такой способ задания производства энтропии TdiS и скорости ее возрастания  широко используется в работах по необратимой термодинамике, нередко без объяснения предпочтительности выбора. В свете изложенного представляется правильным использовать последние выражения (2.228, 2.229) во всех случаях изотермических процессов, но при наличии температурных градиентов и тепловых потоков всегда применять более общие выражения действующих сил: ∇(1/T), ∇(p/T), ∇(μ/T). широко используется в работах по необратимой термодинамике, нередко без объяснения предпочтительности выбора. В свете изложенного представляется правильным использовать последние выражения (2.228, 2.229) во всех случаях изотермических процессов, но при наличии температурных градиентов и тепловых потоков всегда применять более общие выражения действующих сил: ∇(1/T), ∇(p/T), ∇(μ/T).
Выведем еще одно основополагающее соотношение термодинамики необратимых процессов. Обратим внимание на то, что во всех уравнениях скорости возрастания энтропии (или уменьшения термодинамического потенциала) члены, выражающие перенос тепла, изменение объема, перенос вещества, представлены произведениями вида: действующая сила x количество тепла (вещества) в единицу времени:
 . . |
(2.229) |
Тогда, обозначив действующие силы через Х, а количество экстенсивной величины (Q, V, m) в единицу времени через потоки - IQ, IV, Im и т. д. получим для теплопереноса  , для массопереноса , для массопереноса  и т. д. и в общем виде: и т. д. и в общем виде:
 . . |
(2.230) |
Это фундаментальное соотношение необратимой термодинамики связывает скорость производства энтропии с действующими потоками и силами. Оно показывает, что скорость возрастания энтропии пропорциональна произведению действующий силы на поток и в случае действия нескольких потоков они суммируются, давая общую скорость возрастания энтропии в системе.
Уравнение (2.230) иногда записывается в удельных параметрах θv =  , где , где
θv =  . . |
(2.231) |
- скорость возрастания энтропии в единице объема.
Распространена также запись основного уравнения и в виде:
 . . |
(2.232) |
Поскольку  нетрудно видеть, что в этом случае произведение действующих сил на потоки равно скорости уменьшения термодинамического потенциала нетрудно видеть, что в этом случае произведение действующих сил на потоки равно скорости уменьшения термодинамического потенциала
 . . |
(2.233) |
Преимущества такой записи, особенно для изотермических процессов несомненна.
Закон линейных соотношений и принцип взаимности
Закон линейных соотношений устанавливает линейную зависимость любого потока (потока тепла, потока вещества и т. д.) от вызывающих его действующих сил (от градиента температуры, градиентов химических потенциалов и т. д.). Если обозначить поток через I, а действующую силу через Х, то закон линейных соотношений запишется как
 . . |
(2.234) |
где L - коэффициент пропорциональности, называемый кинетическим коэффициентом, или феноменологическим коэффициентом, или коэффициентом переноса. Последнее наименование более точно выражает физическую сущность: L представляет удельное количество экстенсивной характеристики процесса переноса действующей силою через единичное пространство (объем, сечение и т.). Так для диффузии компонента a:
 . . |
(2.235) |
где, очевидно,  - поток компонента a, La - коэффициент переноса - количество вещества а, переносимого через единичное пространство под влиянием - поток компонента a, La - коэффициент переноса - количество вещества а, переносимого через единичное пространство под влиянием  действующей силы диффузии. Если диффундирует несколько компонентов и действующие силы выражены как в (2.235) в соответствии в уравнением скорости возрастания энтропии (см. уравнения 2.208-2.225), то общий поток вещества будет равен сумме потоков остальных компонентов: действующей силы диффузии. Если диффундирует несколько компонентов и действующие силы выражены как в (2.235) в соответствии в уравнением скорости возрастания энтропии (см. уравнения 2.208-2.225), то общий поток вещества будет равен сумме потоков остальных компонентов:
 . . |
(2.236) |
Аналогично для потока тепла (IQ) будем иметь:
 . . |
(2.237) |
Закон линейных соотношений устанавливает также, что в системе, где осуществляется несколько потоков (тепла, вещества и т. д.), они могут быть сложены, если действующие силы выражены в соответствии с уравнением скорости возрастания энтропии. Итак, если в системе происходит перенос тепла и вещества, то общий поток равен:
 . . |
(2.238) |
Обратим внимание, что во всех уравнениях (2.235-2.238) коэффициенты переноса не зависят от действующих сил (условие линейности), тогда как обычные коэффициенты диффузии, теплопроводности имеют сложный нелинейный характер. Покажем это на простом примере изотермической одномерной диффузии, используя <концентрационное> выражение химического потенциала. Диффузионный поток компонента а в этом случае выразится как

Сравнивая это выражение с известным уравнением Фика:  нетрудно видеть, что Da = LaRT / Ca (или La = DaCa / RT) и сколь сложна природа обычного коэффициента диффузии. Еще более сложные соотношения при неизотермической диффузии рассмотрим ниже. нетрудно видеть, что Da = LaRT / Ca (или La = DaCa / RT) и сколь сложна природа обычного коэффициента диффузии. Еще более сложные соотношения при неизотермической диффузии рассмотрим ниже.
Принцип взаимности Онзагера устанавливает соотношение между различными процессами, протекающими в системе одновременно. Он записывается как:
 . . |
(2.240) |
или
 и формулируется: <при соответствующем выборе потоков и сил матрица кинетических коэффициентов симметрична>. Иначе говоря, обнаруживается сходное влияние действующих сил на инородные потоки, если, естественно, эти силы и потоки записаны в соответствии с уравнением скорости возрастания энтропии. Лучше всего проиллюстрировать принцип взаимности на примере. Рассмотрим систему с градиентами температуры и химического потенциала, например, компонента a. Перенос вещества в такой системе будет происходить вследствие градиента химического потенциала (собственно диффузия, или хемодиффузия) и вследствие градиента температуры (термодиффузия). Уравнение потока компонента a запишется в общем виде как:
и формулируется: <при соответствующем выборе потоков и сил матрица кинетических коэффициентов симметрична>. Иначе говоря, обнаруживается сходное влияние действующих сил на инородные потоки, если, естественно, эти силы и потоки записаны в соответствии с уравнением скорости возрастания энтропии. Лучше всего проиллюстрировать принцип взаимности на примере. Рассмотрим систему с градиентами температуры и химического потенциала, например, компонента a. Перенос вещества в такой системе будет происходить вследствие градиента химического потенциала (собственно диффузия, или хемодиффузия) и вследствие градиента температуры (термодиффузия). Уравнение потока компонента a запишется в общем виде как:
| IaM = LaMXaM + LaMQXaQ. |
(2.242) |
или, расшифровывая действующие силы:
 . . |
(2.243) |
Перенос тепла также будет происходить как вследствие градиента температуры, так и вследствие градиента химического потенциала (это явление, обратное термодиффузии, известно как эффект Дюфора).
Уравнение потока тепла выразится в общем виде как:
| IaQ = LaQXaQ + LaQMXaM. |
(2.244) |
и, расшифровывая действующие силы:
 . . |
(2.245) |
Используя соотношение взаимности (2.241), можно записать следующее уравнение:

откуда наглядно видно

что изменение потока вещества, вызванного наложением тепловой силы (градиента температуры), равнозначно изменению потока тепла вследствие наложения градиента химического потенциала компонента. Отнесенные к единице наложенной силы потоки вещества и тепла равны.
Отметим еще раз, что принципы Онзагера - фундаментальные обобщения необратимой термодинамики - справедливы только при соответствующем выборе потоков и сил, который определяется основным уравнением необратимой термодинамики - уравнением производства энтропии.
Стационарные состояния
Особенно эффективно термодинамика необратимых процессов изучает стационарные состояния, т. е. такие, отличные от равновесных состояния, которые не изменяются во времени.
Стационарные состояния, как было впервые показано И. Пригожиным, характеризуются минимальной скоростью возрастания энтропии. Тогда, обозначив для краткости, как это и принято  , условие минимальной скорости возрастания энтропии запишется так: σ = min при IAXA = const, где , условие минимальной скорости возрастания энтропии запишется так: σ = min при IAXA = const, где

а это означает, что

Покажем это простейшим способом. Действительно, если в системе имеется какой-либо стационарный поток и IAXA = const, то минимум энтропии будет выполняться, если другие, сопряженные или вынужденные потоки будут равны нулю. Пусть в схеме возможен вынужденный поток IB, тогда: и

Существуют и более развернутые доказательства тождественности условий минимума скорости возрастания энтропии и равенства нулю всех остальных вынужденных потоков.
Физический смысл этих условий легко пояснить следующим образом. Представим систему в состоянии, когда в ней существуют градиенты интенсивных параметров, например температуры и химических потенциалов каких-либо компонентов. В такой системе должны, очевидно, протекать процессы выравнивания интенсивных параметров, выражаемые потоками тепла и вещества, вплоть до достижения состояния равновесия. Для осуществления стационарного состояния необходимо, чтобы какими-то внешними условиями существования системы градиенты каких-либо параметров, например температуры, были закреплены и поддерживались неизменными во времени ∂XQ/∂t = 0. В таком случае к какому-то моменту в системе протекут все другие естественные процессы, кроме единственного, поддерживаемого наложенным градиентом интенсивного параметра. В нашем примере прекратится перенос вещества, и через систему будет проходить только постоянный стационарный поток тепла, вызванный наложенным на систему градиентом температуры. Мерой отклонения систем от состояния равновесия служит ее энтропия. Энтропия будет возрастать по мере протекания естественных процессов, вплоть до состояния минимальной скорости роста, которое осуществится в стационарных условиях, поскольку все другие процессы, вызывающие возрастание энтропии, будут уже исчерпаны. Как уже отмечалось, из этого вытекает важнейшее свойство стационарных состояний - вынужденные потоки, сопряженные с действием изменяющихся сил, в стационарных системах равны нулю.
В нашем примере это означает, что в системе с наложенным постоянным температурным градиентом потоки вещества, сопряженные с изменяющимися силами ∇(μ/T), равны нулю.
Стационарное состояние, при котором внешними условиями удерживается постоянным (не зависящим от времени) градиент какой-либо одной действующей силы, именуется стационарным состоянием первого порядка. В случае постоянных градиентов каких-либо двух действующих сил осуществляется стационарное состояние второго порядка и т. д. Отметим, что стационарные состояния высших порядков - свыше первого - вполне обычны для природных процессов. В таком случае, соотношение, когда diS/dt = σ = 0 и S = const, можно именовать стационарным состоянием нулевого порядка, которое не что иное как полностью равновесная система с k+2 независимыми параметрами и максимумом энтропии или минимумом термодинамического потенциала системы.
Некоторые приложения термодинамики необратимых процессов
Для иллюстрации приложения методов необратимой термодинамики к природным процессам рассмотрим несколько показательных примеров.
Явления термодиффузии и бародиффузии. Пусть на систему наложен градиент температуры. В соответствии с характером действующих сил градиент температуры будет вызывать изменение химических потенциалов компонентов и диффузию вещества. В свою очередь термодиффузия будет приводить к изменению концентрации компонентов и вследствие этого вызывать противодействующую ей концентрационную диффузию, или хемодиффузию компонентов, стремящуюся ликвидировать градиент концентрации, вызванной термодиффузией. Для какого-либо компонента а общий поток выразится как
 . . |
(2.251) |
где  - поток, кинетический коэффициент (или коэффициент переноса) и действующая сила термодиффузии; - поток, кинетический коэффициент (или коэффициент переноса) и действующая сила термодиффузии;  - поток, кинетический коэффициент и действующая сила хемодиффузии. Раскроем выражение действующих сил. - поток, кинетический коэффициент и действующая сила хемодиффузии. Раскроем выражение действующих сил.
Выше была показана зависимость химического потенциала от других факторов состояния, которое мы выразим в концентрационной форме:
 . . |
(2.252) |
Ограничившись идеальными изобарическими условиями (dp = 0, γa* = 1), выражая в общем виде изменение параметров в градиентах и обозначая эффективный член химического потенциала RT lnCa через (∇σa)p,T, получим:
| ∇σa = -Sa∇T + (∇σa)p,T. |
(2.253) |
В соответствии с уравнениями возрастания необратимой энтропии (уравнение 2.207) действующая сила диффузии в термоградиентных условиях выразится следующим образом:

(При выводе уравнения (2.254) использовано уравнение (2.243) и соотношение (2.86): Ha = μa + TSa).
Действующая сила термодиффузии  , поскольку эта сила наложена на систему и на нее не влияют процессы, происходящие внутри системы (это принципиально важно). , поскольку эта сила наложена на систему и на нее не влияют процессы, происходящие внутри системы (это принципиально важно).
Подставляя действующие силы в уравнение (2.250), получим:

- выражение потока компонента в поле градиента температуры и химического потенциала компонента.
Для стационарных условий, в которых  , из уравнений (2.255) имеем: , из уравнений (2.255) имеем:

Заменяя (∇σa)p,T на RT∇lnCa. получим:

Уравнение (2.257) показывает, как изменится концентрация компонента а при наложении на систему температурного градиента. 3аметим, что общая тенденция связана с термодинамическим параметром - энтальпией компонента, тогда как фактическое распределение определяется в существенной мере кинетическими характеристиками LM и LMQ.
Если представить уравнение (2.257) в обычной дифференциальной форме, преобразуя получим соотношение

где  - коэффициент термодиффузии, а - коэффициент термодиффузии, а  - коэффициент диффузии (хемодиффузии) компонента а. - коэффициент диффузии (хемодиффузии) компонента а.
Уже обращали внимание, насколько сложна в действительности природа и зависимость от различных параметров таких обычных характеристик, как коэффициенты диффузии и термодиффузии.
Относительное разделение двух компонентов многокомпонентного расплава, раствора или газовой смеси можно оценить, сопоставляя потоки Ia и Ib. В стационарном состоянии ∑I = 0, Ia = Ib. Тогда (опускаем математические выкладки) в соответствии с (2.258) выражая в обычной дифференциальной форме получим

где величины Qa* и Qb* иногда называются теплотами переноса компонентов. Уравнение (2.259) показывает, что в поле градиента температур будет происходить непременное разделение компонентов, причем направленность и интенсивность этого процесса определяются термодинамическими и кинетическими характеристиками компонентов. В общем случае, учитывая, что LM >> LMQ, высокотемпературные части системы будут обогащаться компонентами с большими энтальпиями (или энтропиями) и с большими кинетическими коэффициентами диффузии, или, иначе говоря, с большими теплотами переноса.
Аналогично образом можно рассмотреть явления бародиффузии, т. е. диффузии, вынужденной наложенным градиентом давления:
| Ia = IaA + IaM = LaMAXA + LaMXM. |
(2.260) |
В стационарных изотермических условиях (влияние термодиффузии мы рассмотрели выше):

где ∇μ = Va∇p + RT∇lnCa при γa* = 1.
Откуда для стационарного состояния следует:

Выражая (2.262) в обычной дифференциальной форме получим

где  - как и выше коэффициент хемодиффузии компонента, - как и выше коэффициент хемодиффузии компонента,
| - (LaMVa + LaMA) = Dap. |
(2.264) |
- коэффициент бародиффузии компонента. Рассматривая разделение компонентов а и b для стационарного состояния: Ia = Ib, получим (опуская промежуточные преобразования):
 . . |
(2.265) |
где  - можно обозначить как <работу переноса> в поле градиента давлений. - можно обозначить как <работу переноса> в поле градиента давлений.
Из приведенных уравнений видно что зоны повышенного давления будут обогащаться компонентами с меньшими мольными объемами, меньшими <работами переноса> и большими кинетическими коэффициентами диффузии.
Уравнения термо- и бародиффузии лежат в основе моделирования разделения компонентов в значительных гомогенных массах расплавов, например в длительно существующих больших магматических камерах. Однако это справедливо, если ∇T и ∇p невелики, чтобы в системе не возникало конвекции или гетерогенизации.
Реально крупные магматические камеры в литосфере находятся в более сложной обстановке, когда независимыми параметрами их существования являются и градиент температуры и градиент давлений. В этих условиях поток вещества будет определяться наложенными действующими силами - градиентом давления и вынужденным потоком хемодиффузии, действующие силы которой ( ) зависят от температуры, давления и концентрации компонентов. Тогда, например, для потока компонента а получим следующую зависимость: ) зависят от температуры, давления и концентрации компонентов. Тогда, например, для потока компонента а получим следующую зависимость:

Раскрывая выражения действующих сил и разумно преобразуя получаемое выражение мы получим обычную зависимость Ia от обозначенных параметров (мы не приводим эти преобразования, оставляя их для самостоятельных упражнений читателей). При этом следует иметь в виду следующие важные соотношения: градиент температуры  является наложенной силой и поэтому не зависит ни от каких-либо других параметров; в выражении является наложенной силой и поэтому не зависит ни от каких-либо других параметров; в выражении  градиент давления ∇p также является независимой наложенной силой и в соответствующем выражении температуры должна быть вынесена из под знака градиента градиент давления ∇p также является независимой наложенной силой и в соответствующем выражении температуры должна быть вынесена из под знака градиента  , если ее изменениями можно пренебречь; и, напротив, , если ее изменениями можно пренебречь; и, напротив,  - зависимый параметр и его значение должно быть раскрыто, как это сделано выше, причем - зависимый параметр и его значение должно быть раскрыто, как это сделано выше, причем  (см. 2.252, 2.253 и 2.261). (см. 2.252, 2.253 и 2.261).
Для стационарных условий Ia = 0, которые будут уже стационарными условиями второго порядка, получим соотношение:

которое показывает изменение концентрации компонента а в одномерном пространстве под действием двух наложенных и одной вынужденной действующих сил. Сопоставляя (2.267) с уравнениями (2.258) и (2.263) убедимся, что полученное уравнение (2.267) можно с известным приближением представить в виде
 . . |
(2.268) |
Исследования инфильтрации и диффузии при метасоматических процессах могут служить ярким примером приложения методов необратимой термодинамики. Метасоматические процессы9 представляют сложные природные явления, вызываемые воздействием на горные породы неравновесных с ними гидротермальных растворов. Общий поток например компонента а выразится как:

где Iaint - поток компонента а, вызванный течением раствора, Iadif - диффузионный поток компонента а, Ia∇T - перемещение компонента а вследствие температурного градиента, Iakin - наложение на поток компонента а кинетических факторов, связанных со скоростями реакции взаимодействия раствора и твердой породы.
Общее решение уравнения (2.269) является далеко не ординарной задачей, поэтому ограничимся уже рассмотренным нами более простым случаем изотермического процесса Ia∇T = 0 в условиях локального равновесия между раствором и горной породой Iakin = 0.
Тогда поток инфильтрации и диффузии компонента а выразится как:
 . . |
(2.270) |
Раскроем значение кинетических коэффициентов (коэффициентов переноса) и действующих сил. Для инфильтрации: а) в одномерном пространстве  ; б) выражение ∂p/∂x получим из уравнения Пуазейля: ; б) выражение ∂p/∂x получим из уравнения Пуазейля:  , где ν - скорость фильтрации, η - вязкость, k -характеристики фильтра, отражающие его проницаемость, Δp/Δl - <гидравлический уклон>, равный в каждой точке ∂p/∂x; тогда действующая сила ∂p/∂x может быть заменена в соответствии с уравнением Пуазейля скоростью фильтрации w0 в данной среде (с учетом k и η0), т. е. , где ν - скорость фильтрации, η - вязкость, k -характеристики фильтра, отражающие его проницаемость, Δp/Δl - <гидравлический уклон>, равный в каждой точке ∂p/∂x; тогда действующая сила ∂p/∂x может быть заменена в соответствии с уравнением Пуазейля скоростью фильтрации w0 в данной среде (с учетом k и η0), т. е.  ; в) Lainf выражает количество вещества, перенесенного в единицу времени через сечение. Оно равно концентрации компонента а в растворе при данной температуре (тем самым учитывается, что La(T)inf взят при определенной температуре) т. е. Cainf - в том случае, если компонент переносится с одинаковой для раствора скоростью; г) если же имеет место фильтрационный эффект, т. е. скорость фильтрации компонента а (wa) отлична от скорости фильтрации растворителя (w0), то La(T)inf = φaCa, где φa - коэффициент фильтрационного эффекта φa = wa/w0; д) таким образом: ; в) Lainf выражает количество вещества, перенесенного в единицу времени через сечение. Оно равно концентрации компонента а в растворе при данной температуре (тем самым учитывается, что La(T)inf взят при определенной температуре) т. е. Cainf - в том случае, если компонент переносится с одинаковой для раствора скоростью; г) если же имеет место фильтрационный эффект, т. е. скорость фильтрации компонента а (wa) отлична от скорости фильтрации растворителя (w0), то La(T)inf = φaCa, где φa - коэффициент фильтрационного эффекта φa = wa/w0; д) таким образом:
 . . |
(2.271) |
Для диффузии: а) в одномерном пространстве  ; б) раскрывая это выражение так, как это было сделано выше, получим: ; б) раскрывая это выражение так, как это было сделано выше, получим:

уравнение диффузионного потока в терминах концентрации и коэффициента диффузии.
Суммируя уравнения (2.271) и (2.272) в соответствии с (2.270), получим
 . . |
(2.273) |
Для многокомпонентного раствора будем иметь k уравнений вида (2.273), которые, будучи сложены вследствие закона линейных соотношений, образуют общий поток вещества. Доказано10, что в условиях локального равновесия система из k уравнений может быть сведена к одному уравнению, описывающему скорость перемещения сечения, в котором происходит реакция замещения одного или нескольких минералов другим или несколькими другими. Упрощенно, обозначая через U скорость перемещения сечения, можно записать:
 . . |
(2.274) |
где существенно направление диффузии относительно инфильтрации. Очевидно, что в случае встречной диффузии Udif имеет смысл, если Udif > Uinf. При сонаправленной диффузии, как показывают расчеты, основанные на экспериментальных данных, диффузионный член оказывает влияние, если Uinf > Udif не более, чем на 1,0-1,5 порядка: при Uinf >> Udif на два порядка происходит полное подавление сонаправленной диффузии.
Примечательным открытием при теоретическом анализе уравнений метасоматизма оказалось, что возникновение сечений, где осуществляются реакции замещения, обусловлено дифференциальной подвижностью компонентов: в предельном случае k-компонентной системы возникает метасоматическая колонка из k+1 зоны, на которой один из компонентов переходит из инертного во вполне подвижное состояние. При этом происходит уменьшение числа минералов в каждой из последующих зон, вплоть до тыловой, минеральной зоны (вспомним, что согласно правилу фаз (уравнение 2.56), в изотермо-изохорических системах с вполне подвижными компонентами rT,V,μ = k + 1). Основная зональность с изменением числа фаз на границе зон может осложниться дополнительной зональностью с одинаковым числом минералов в сопредельных зонах в тех случаях, когда при выносе или привносе компонентов возможна больше чем одна реакция раствора с замещенной породой. Для дополнительной реакционной зональности особенно благоприятны диффузионные зоны.
Установлено принципиальное различие, и, следовательно, критерии отличия инфильтрационных и диффузионных зон: в пределах инфильтрационных зон и состав зон и состав раствора остаются постоянными, в пределах диффузионных зон вследствие переменного градиента концентраций состав раствора непрерывно изменяется, соответственно переменным оказывается и состав минералов - твердых растворов. Для чисто инфильтрационных колонок (Udif = 0) на границах зон происходит резкое скачкообразное изменение концентрации раствора и химического состава зон. В диффузионных колонках на границах зон происходит изменение градиента концентраций, изменение химического состава зависит от минерального состава зон и минеральных реакций на границах и может происходить как постепенно, так и скачкообразно (особенно в случае минералов постоянного состава).
Отмеченные здесь и другие важные черты строения метасоматических колонок, полученные путем анализа теоретических моделей метасоматизма, получили полное подтверждение при экспериментальном моделировании метасоматизма и изучении разнообразных природных метасоматитов. Это в корне изменило все изначальные представления о метасоматитах и составляет в настоящее время фундаментальную основу для понимания строения и генезиса этих своеобразных пород, имеющих важнейшее значение для формирования пород литосферы и образования многих типов минеральных месторождений. Для освоения физической геохимии метасоматизма следует обратиться к специальным работам.
Химическое сродство реакций - следующий пример приложения методов термодинамики необратимых процессов. Оно характеризует условия протекания необратимых химических реакций в системе.
Рассмотрим в качестве примера изотермо-изобарическую систему. Ее термодинамический потенциал:
 . . |
(2.32) |
и в условиях постоянных температуры и давления:
 . . |
(2.275) |
Необратимое изменение термодинамического потенциала, как было показано выше, равно:
 . . |
(2.276) |
или для конечных приращений
 . . |
(2.277) |
Представление о химическом сродстве вводится соотношением  и постулируется Де-Донде, который ввел это в термодинамику, зависимостью и постулируется Де-Донде, который ввел это в термодинамику, зависимостью
 . . |
(2.278) |
где  - координата реакции, а А - химическое сродство. Координата реакции, называемая также степенью полноты реакции или степенью превращения реакции, представляет количество вещества, принявшего участие в реакции. Если, допустим, протекает реакция - координата реакции, а А - химическое сродство. Координата реакции, называемая также степенью полноты реакции или степенью превращения реакции, представляет количество вещества, принявшего участие в реакции. Если, допустим, протекает реакция
| νAA + νBB → νCC + νDD. |
(2.279) |
где νA...νD - стехиометрические коэффициенты, показывающие эквивалентные количества молей вещества, то
 . . |
(2.280) |
количество прореагировавшего вещества, отнесенное к стехиометрическому коэффициенту, одинаково для всех веществ и показывает степень протекания (координату) реакции. Действительно, например, для реакции образования форстерита: 2MgO + SiO2 = Mg2SiO4, где νSiO2 = -1, νMgO = -2, νMg2SiO4 = 1 получим
 . . |
(2.280) |
Из уравнения (2.280) следуют важные соотношения:
Проинтегрировав любое из уравнений (2.281) получим
 |
(2.282) |
поскольку  . И скорость реакции v выразится как . И скорость реакции v выразится как
 |
(2.283) |
Раскроем теперь выражение химического сродства. В соответствии с (2.277) и (2.278)
 . . |
и
 , , |
или
 , , |
(2.284) |
где индекс i у потенциала обычно опускают, так как координата реакции ε безусловно обозначает необратимое изменения свободной энергии. В свою очередь11
 , , |
(2.285) |
откуда следуют важные соотношения:
 , , |
(2.286) |
 , , |
(2.287) |
Уравнения (2.285)-(2.287) показывают, что химическое сродство является величиной обратной свободной энергии реакции и при A = -ΔG = 0 естественным образом протекает химическая реакция вплоть до в состоянии равновесия.
Выведенные соотношения могут быть выражены в общепринятых терминах потоков и действующих сил. Как было показано,
 , , |
(2.230) |
или в другой записи
 , , |
(2.233) |
тогда для потока вещества в химической реакции будем иметь:
 , ,
где I = dε/dt - поток, A = X - действующая сила. Уравнение (2.288) может быть представлено также в виде:
 , , |
(2.289) |
где v = dε/dt - скорость реакции. В случае записи возрастания энтропии как в уравнении (2.230) температура войдет в выражение действующей силы (X = A/T):
 , , |
(2.290) |
В заключение отметим, что выражение химических реакций методами необратимой термодинамики обстоятельно разработано учеными бельгийской школы, особенно Де-Донде и его учениками И. Пригожиным и Р. Дефеем. Суть основополагающего перехода состоит в введении химического сродства и замене переменной dm на vdε. Действительно, для закрытой системы, например изотермо-изобарической G = ƒ(p, T, mao...mko) можно выразить ее потенциал через G = ƒ(p, T, mao...mko), где mao...mko = const и  . Тогда факторами состояния оказываются G = ƒ(p, T, ε) и изменение свободной энергии выразится через . Тогда факторами состояния оказываются G = ƒ(p, T, ε) и изменение свободной энергии выразится через
| dG = -SdT + Vdp - Adε |
(2.291) |
Сходным образом могут быть получены и другие термодинамические потенциалы:
dU = TdS - pdV - Adε
dH = TdS + Vdp - Adε
dF = -SdT - pdV - Adε |
(2.292) |
откуда

и могут быть получены все другие термодинамические зависимости. Описание химических процессов как необратимых через химическое сродство и координаты реакции имеет и свои преимущества, и трудности. Однако более подробное изложение этих вопросов выходит за рамки настоящей книги.
1 - Можно показать это иначе следующей алгебраической подстановкой: δU = δQ - δAΣ, где член -δAΣ включает механическую работу выполненную системой -δA, имеющую отрицательный знак, поскольку она уменьшает внутреннюю энергию системы и член +δW, включающий всю химическую работу системы, увеличивающую ее внутреннюю энергию в результате привноса вещества, тепла химических реакций и т. д. Тогда -δAΣ = -δA+δW и подставляя δU = δQ - δAΣ = δQ-δA+δW получим выражение (2.7). При этом важно, что механическая работа, совершаемая системой и <химическая работа>, передаваемая системе, имеюm как принято в термодинамике, разные знаки. Вверх
2 - Заметим, что для сложных термодинамических систем вместо (2.7) справедливо выражение δU = δQ - δAΣ = δQ-δA+δW+ΣδZ (2.7а), где ΣδZ - сумма других <работ> системы, где знак δZ будет положительным, если работа передает энергию системе, и, напротив, отрицательным, если работу совершает сама система. Вверх
3 - Действительно, в изотермо-изохорической системе не может происходить уменьшение энергии за счет выравнивания температур, поскольку температура задана неизменной для всех фаз системы условиями существования и является независимым (интенсивным) фактором состояния. Уменьшение свободной энергии возможно лишь за счет механической работы: dF=-(pAdV-pBdV = (pB-pA)dV < 0, где pA > pB и dF = -μAadma + μBadma = (μBa - μAa)dma < 0, где μAa > μBa для всех k компонентов. Отсюда следует что k+1 интенсивный параметр должен быть выровнен по фазам

Иначе говоря, (k+1)r возможная вариация факторов состояния связана (k+1)(r-1) уравнением, и независимыми остаются k+1 параметра - экстенсивные факторы равновесия V, ma...mk, таким образом факторы состояния системы:
ƒ = ƒin + ƒex = 1 + (k+1) = k + 2. Вверх
4 - Отметим, что в связи с происходившими дискуссиями по этому поводу имеется даже специальное решение комиссии по химической термодинамике (Коржинский 1972). Вверх
5 - Здесь и в дальнейшем мы будем пользоваться, как и принято, более краткой записью термодинамических потенциалов, опуская δQi и равенство нулю, но всегда помня об условиях равновесия систем. Вверх
6 - Нетрудно убедиться, дифференцировав (2.81)  . В то же время, обозначив массу системы для краткости через M и умножив (2.81) на M, получим . В то же время, обозначив массу системы для краткости через M и умножив (2.81) на M, получим  или или  и мольная доля в системе выступает как экстенсивный параметр выражений в относительных количествах. Вверх и мольная доля в системе выступает как экстенсивный параметр выражений в относительных количествах. Вверх
7 - Для иллюстрации рассмотрим простенькую моновариантную реакцию андалузит (Andl) = муллит (Mul) + кварц(Q) в двухкомпонентной системе Al2O3-SiO2 (r=k+1=3).
|
VAndl mAndlAl2O3 mAndlSiO2 |
|
VAndl 1 1 |
|
|
| DV3 = |
VMul mMulAl2O3 mMulSiO2 |
= |
VMul 3 2 |
= |
3VAndl - VMul - VQ |
|
VQ mQAl2O3 mQSiO2 |
|
VQ 0 1 |
|
|
аналогичным образом
|
SAndl mAndlAl2O3 mAndlSiO2 |
|
|
| DS3 = |
SMul mMulAl2O3 mMulSiO2 |
= |
3SAndl - SMul - SQ |
|
SQ mQAl2O3 mQSiO2 |
|
|
и
.
Вверх
8 - Заметим, что некоторые термодинамисты вводят нулевой закон термодинамики, определяющий температуру как меру теплового равновесия и начало ее исчисления - абсолютный нуль, однако освещение этих вопросов уходит далеко в область <чистой> термодинамики и теоретической физики. Вверх
9 - Напомним, что метасоматическими процессами илиметасоматозом называются процессы преобразования горных пород и руд, происходящие путем замещения одних минералов другими, протекающие с изменением химического состава пород или руд с сохранением их твердого состояния в целом под воздействием гидротермальных растворов. Вверх
10 - см. работы по теории метасоматической зональности: Коржинский 1951, 1969; Жариков 1961,1965, 1998 и др., поскольку подробное изложение этих вопросов выходит за рамки книги. Вверх
11 - Заметим, что вместо  здесь, как принято в термодинамике химического сродства, использовано здесь, как принято в термодинамике химического сродства, использовано  где μa - значение химического потенциала, отличное от равновесного (μaeq), поскольку в Δμa = μa - μaeq, μaeq равны по всем фазам системы. Вверх где μa - значение химического потенциала, отличное от равновесного (μaeq), поскольку в Δμa = μa - μaeq, μaeq равны по всем фазам системы. Вверх
|

